药物性肝损伤已成为一个热点性问题。药物在肝脏中会通过酶促过程进行生物转化,并伴有自由基的产生,这也是药物诱导产生肝毒性的主要原因。然而,具有有限穿透力的发光成像难以对病变位置的自由基进行定位成像。湖南大学宋国胜教授开发了一种基于普鲁士蓝(PB)的可激活纳米探针,它可以结合磁共振成像(MRI)和光声成像(PAI)对深部组织中的ONOO-进行成像。
本文要点:
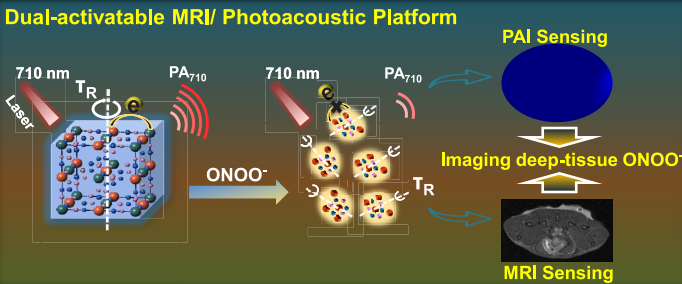
(1)实验发现ONOO-可以将PB内的FeII氧化成FeIII,同时破坏PB的晶体结构,进而使得PB在710 nm处的强吸收大大减弱。因此,PB降低的光声成像(PA)信号可以作为检测ONOO-的指标。与此同时,与ONOO-反应后,PB的尺寸会减小导致其旋转相关时间(τR)减小,导致产生可用于感知ONOO-的MRI信号。
(2)最后,实验也证明了PB纳米探针能够通过PAI和MRI双模态成像成功地对药物诱导的肝毒性所产生的ONOO-变化情况进行体内成像。值得注意的是,这种双模态成像的互补性使得该探针不仅可以对药物性肝损伤中的ONOO-进行准确的可视化,而且也为识别肝损伤区域提供了重要的解剖学结构信息。
Fangfang Chen. et al. Activatable Magnetic/Photoacoustic Nanoplatform for RedoxUnlocked Deep-Tissue Molecular Imaging In Vivo via Prussian Blue Nanoprobe. Analytical Chemistry. 2020
DOI: 10.1021/acs.analchem.0c02859



















