嵌合抗原受体(CAR)工程化的T细胞(CAR-Ts)治疗在癌症治疗中具有出色的功效,尤其是在血液系统恶性肿瘤的治疗中效果显著。不幸的是,由于缺乏肿瘤特异性抗原而产生的脱靶效应和肿瘤微环境引起的免疫抑制,使其在实体肿瘤中的应用受到挑战。
于此,中国药科大学徐寒梅、薛建鹏等人构建了一个可切换的双受体CAR-T细胞(sdCAR-T),其活性依赖于双重抗原(间皮素和异硫氰酸荧光素),并由“开关”(FPBM)严格控制,该开关由PD-L1阻断肽欧联异硫氰酸荧光素组成。
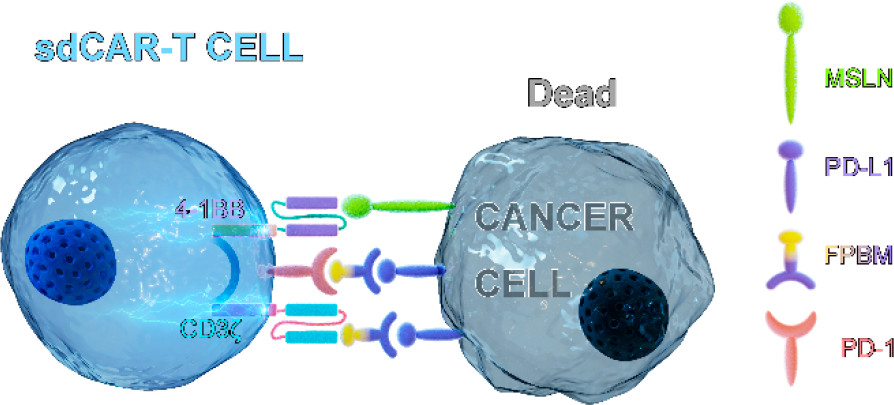
本文要点:
1)仅当FPBM和表达PD-L1和间皮素的同源肿瘤细胞共存时,SdCAR-T细胞才被激活。
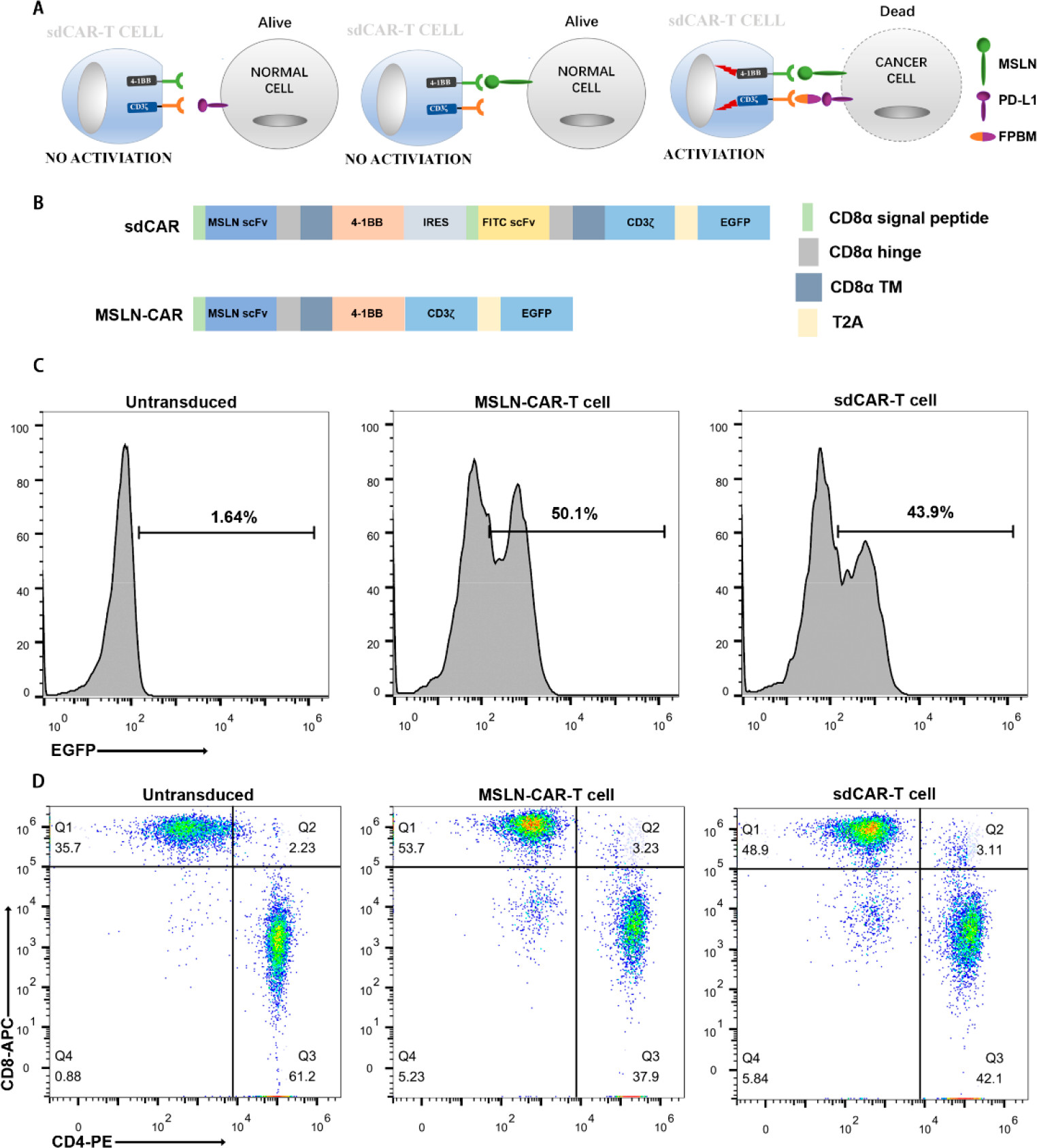
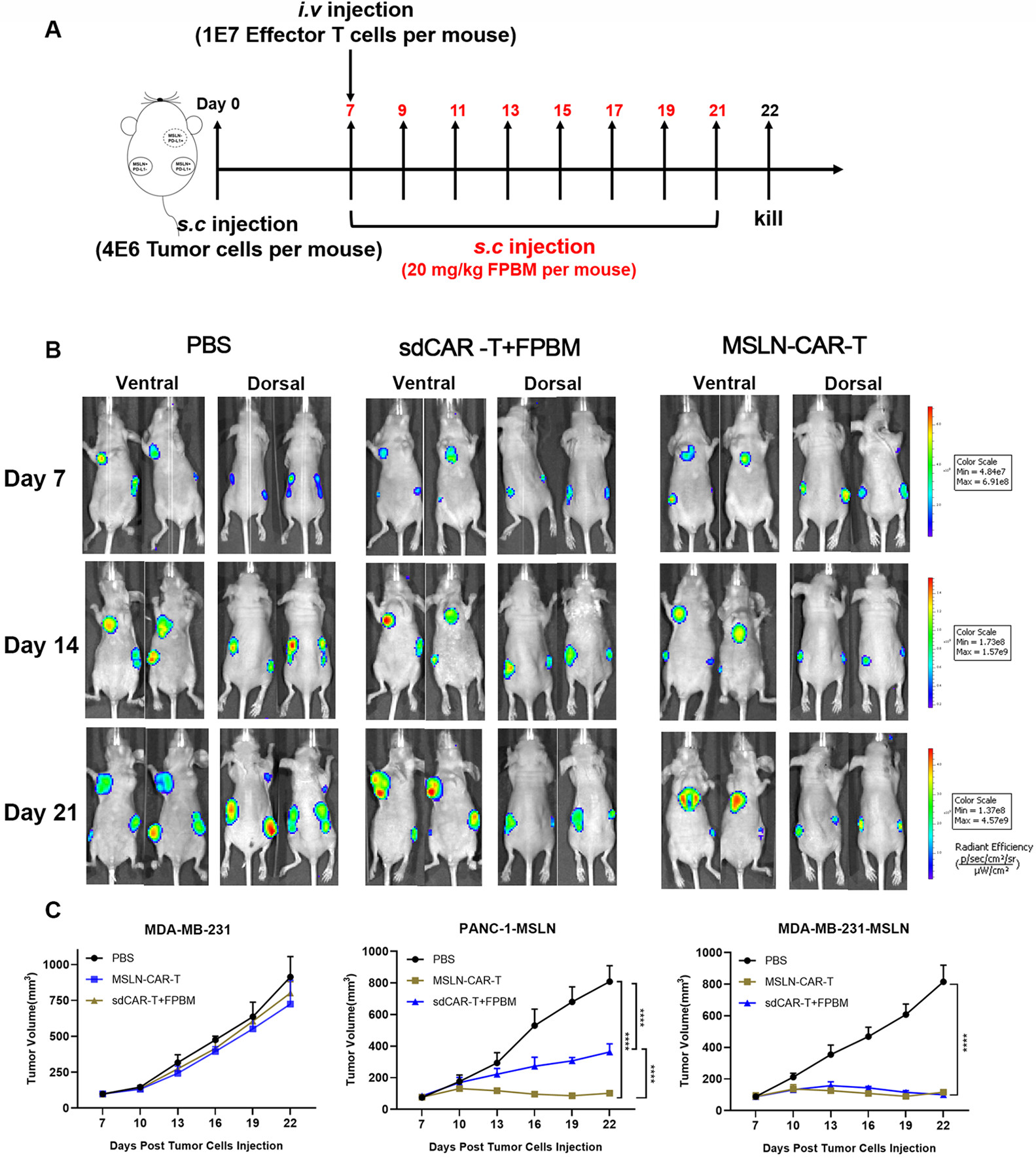
2)重要的是,与第二代间皮素CAR-T细胞相比,体外长期增殖实验和体内药效学研究显示该系统具有更强的抗肿瘤活性。鉴于这种新颖的治疗范例比传统的CAR-T细胞更安全,更有效,它可能成为治疗实体瘤的新策略。
参考文献:
Peiwei Yang, et al., Enhanced Safety and Antitumor Efficacy of Switchable Dual Chimeric Antigen Receptor-Engineered T Cells against Solid Tumors through a Synthetic Bifunctional PD-L1-Blocking Peptide. Journal of the American Chemical Society 2020.
DOI: 10.1021/jacs.0c08538
https://pubs.acs.org/doi/abs/10.1021/jacs.0c08538


















