锂氧(Li-O2)电池因其高能量密度而引起了广泛的研究兴趣。除了Li2O2(Li-O2电池中典型的放电产物)以外,LiOH也被证明具有电化学活性。
有鉴于此,美国阿贡国家实验室Khalil Amine,陆俊教授报道了一种简单的策略,通过在锂电解质中使用阳离子添加剂Na+来用于可逆的LiOH基Li-O2电池。
文章要点
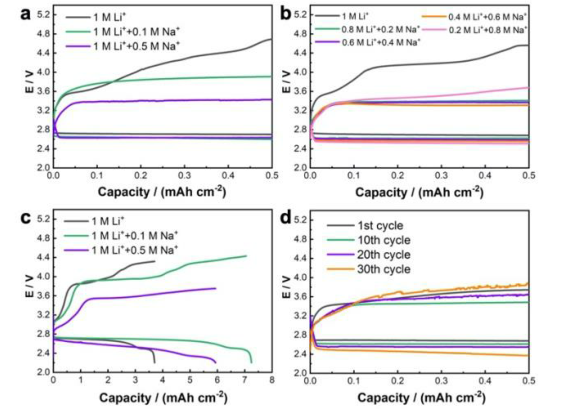
1)使用非锂阳离子的目的是改变溶剂化环境和电解质中的平衡,并使反应路径重新导向LiOH的形成。因此,在电池中没有氧化还原介体的情况下,LiOH被检测为唯一的放电产物,同时LiOH充电电位从超过4.0 V降低至3.3 V。此外,在正极表面没有观察到任何钠基物种。
2)研究表明,钠离子会改变电解质中锂离子的溶剂化环境,并可能在第一次放电过程中促进电解质降解而形成LiOH,但在随后的循环中不会出现明显的电解质分解。
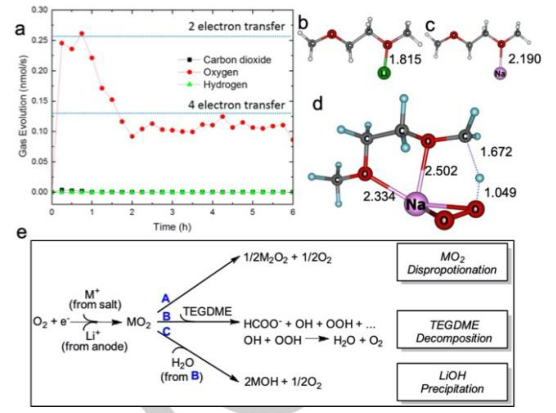
3)研究人员通过理论研究分析了可逆LiOH形成和分解的机理。使用密度泛函理论计算醚溶剂与Na+和Li+的键长。Na-O距离(2.19 Å)比与四甘醇二甲醚(TEGDME)配合物中的Li-O距离(1.82 Å)长,与Li+离子相比,这表明电极附近的Na+离子围绕溶剂分子可能会产生更像气相的环境。此外,双层中Na离子的存在将通过NaO2参与甲酸盐,OH和OOH的形成来增强电极表面附近的“气相”环境。计算表明,在NaO2参与过渡态的解决方案中,C-H途径的势垒仅为0.91 eV,远低于没有NaO2的势垒(1.58 eV)。随后,OH和OOH产物可通过OH从TEGDME提取H或通过OOH与OH反应生成H2O和O2,生成的H2O在放电过程中的LiOH形成中起关键作用。
通过设计促进LiOH形成/分解的简单系统来调节Li-O2电池的电池化学具有重要意义。
Xuanxuan Bi, et al, Cation additive enabled rechargeable LiOH based lithium-oxygen batteries, Angew. Chem. Int. Ed.
DOI:10.1002/anie.202010745
https://doi.org/10.1002/anie.202010745



















