血栓形成是各种危及生命的心血管疾病的主要原因。然而,由于半衰期短、对血栓部位靶向性低以及意外出血并发症,目前使用药物的抗血栓治疗效果有限。考虑到血栓的生物学特性,包括过氧化氢(H2O2)的上调和纤维蛋白的丰富性,美国威斯康星大学麦迪逊分校宫绍琴教授等人设计了一种H2O2响应性纳米载体,用于抗血栓药(即替罗非班)的靶向血栓递送。
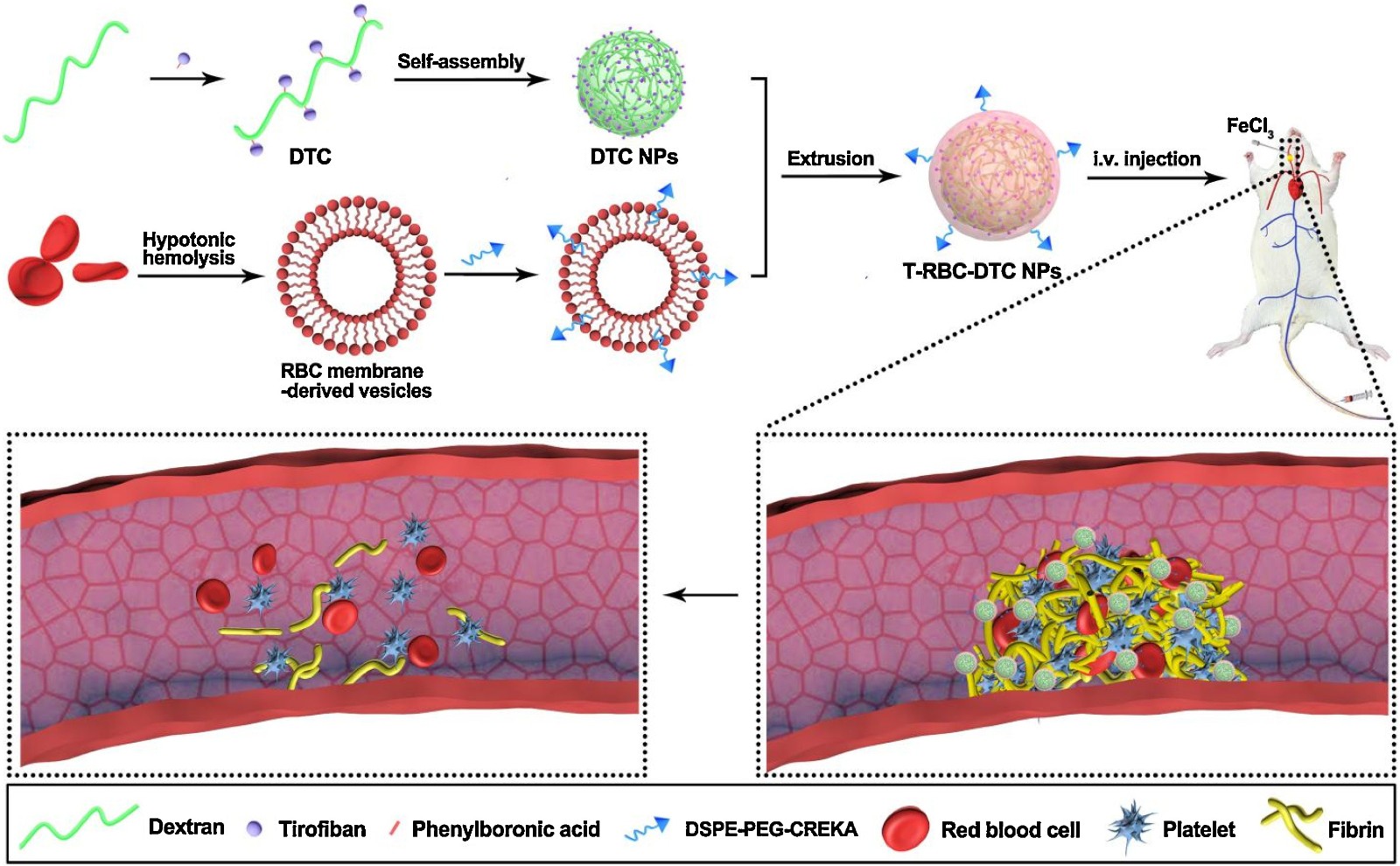
本文要点:
1)该纳米载体由药物偶联葡聚糖纳米核和红细胞膜壳组成,表面修饰纤维蛋白靶向肽CREKA。其中,抗血栓药物替罗非班通过H2O2可裂解的苯基硼酸酯键与葡聚糖偶联。纤维蛋白靶向的红细胞膜掩蔽葡聚糖-替罗非班结合物纳米粒子(即T-RBC-DTC-NPs)可清除H2O2并提供替罗非班的控制释放,以实现特定部位的抗血栓作用。
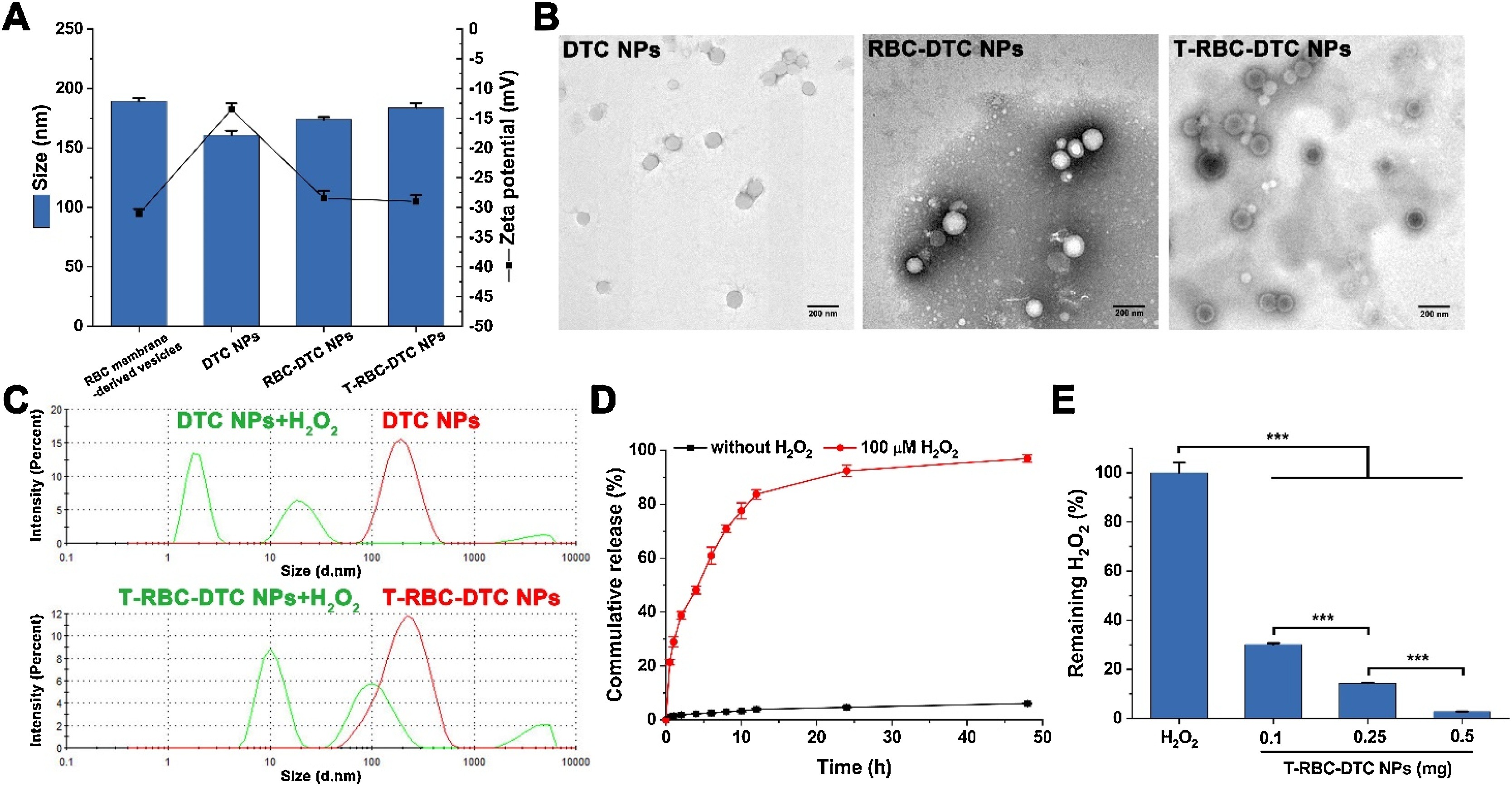
2)在RAW 264.7细胞和HUVECs中,T-RBC-DTC-NPs能有效清除H2O2并保护细胞免受H2O2诱导的细胞毒性。在氯化铁诱导的颈动脉血栓形成小鼠模型中,与游离药物相比,T-RBC-DTC NP有效地积聚在受伤的颈动脉上,并表现出明显增强的抗血栓活性。组织学分析显示T-RBC-DTC-NPs具有良好的生物相容性。
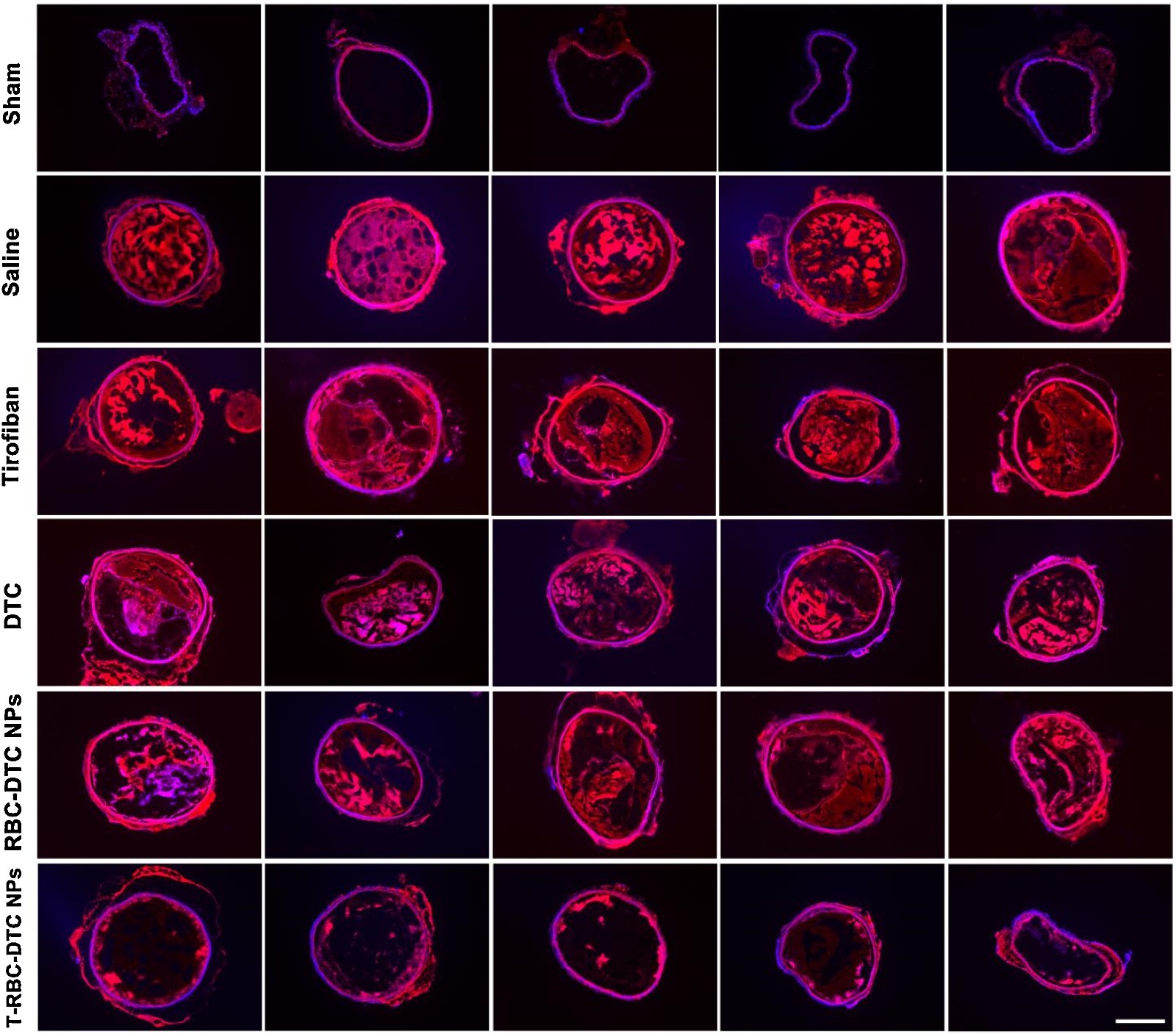
综上所述,该结果表明,这种生物工程纳米载体为血栓性疾病提供了一种有前途的治疗策略。
参考文献:
Yi Zhao, et al., Biomimetic fibrin-targeted and H2O2-responsive nanocarriers for thrombus therapy. Nano Today 2020.
https://doi.org/10.1016/j.nantod.2020.100986


















