CRISPR-Cas技术可对真核生物和原核生物的基因进行编程编辑。然而,前导Cas9和Cas12a酶对于大型删除的能力仍然有限。有鉴于此,美国加州大学旧金山分校的Joseph Bondy-Denomy等研究人员,提出了一个紧凑的Cascade-Cas3系统有针对性的基因工程。
本文要点
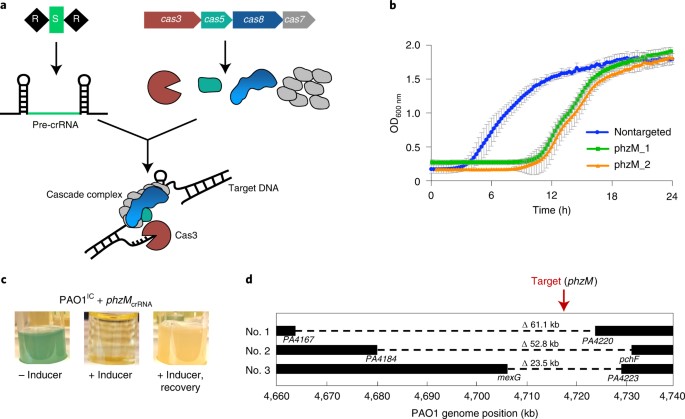
1)研究人员使用进行性核酸酶Cas3以及最小的基于I-C类型Cascade酶系统在细菌中进行靶向基因组工程。单个CRISPR RNA引导下的DNA解理可以产生大的删除(7 - 424 个碱基),在铜绿假单胞菌中能达到将近100%的效率,而Cas9只产生小的删除和点突变。
2)Cas3产生开始于编程位点的双向删除,可以实现减少铜绿假单胞菌基因组的837 kb (13.5%)。大型删除的边界可以在Cascade-Cas3编辑过程中被同源进化修复模板有效识别,然而Cas9不行。
3)可转移的“多合一”载体可在大肠杆菌、丁香假单胞菌和肺炎克雷伯菌中发挥作用,并且内源性CRISPR-Cas通过“抗-抗-CRISPR”策略得到了增强。
本文研究表明,铜绿假单胞菌I-C类型Cascade-Cas3 (PaeCas3c)促成快速菌株操纵,在合成生物学、基因组最小化和消除大型基因组区域都有应用。
参考文献:
Blint Csrg, et al. A compact Cascade–Cas3 system for targeted genome engineering. Nature Methods, 2020.
DOI:10.1038/s41592-020-00980-w
https://www.nature.com/articles/s41592-020-00980-w


















