活性氧(ROS)介导的抗肿瘤治疗具有肿瘤特异性、疗效高、毒副反应低等优点,因此其在肿瘤治疗中具有良好的应用潜力。但是,肿瘤微环境(TME)的乏氧和光敏剂渗透性低等问题也限制了其在临床的进一步应用。暨南大学刘杰教授和叶刚教授构建了一种由介孔二氧化硅纳米粒子(MS)核和MnO2壳组成的复合核壳结构纳米酶(MS-ICG@MnO2@PEG),并将其用于ROS介导的癌症治疗。
本文要点:
(1)一方面,MS-ICG@MnO2@PEG可以催化H2O2产生O2以增强光动力治疗(PDT),另一方面,它也可通过消耗GSH以触发类芬顿反应生成·OH,进而增强化学动力治疗(CDT)。在细胞水平上,MS-ICG@MnO2@PEG纳米酶具有良好的生物相容性,并可在4T1肿瘤细胞中诱导产生ROS,破坏肿瘤细胞中的氧化还原平衡,影响其线粒体功能进而特异性杀死肿瘤细胞。
(2)体内实验结果表明,MS-ICG@MnO2@PEG纳米酶可选择性地在4T1肿瘤小鼠的肿瘤部位聚集,进而抑制肿瘤的生长和转移。因此,这一研究表明该核-壳结构纳米酶可以作为ROS介导的癌症治疗的有效平台,增强PDT和CDT联合治疗乳腺癌的效果。
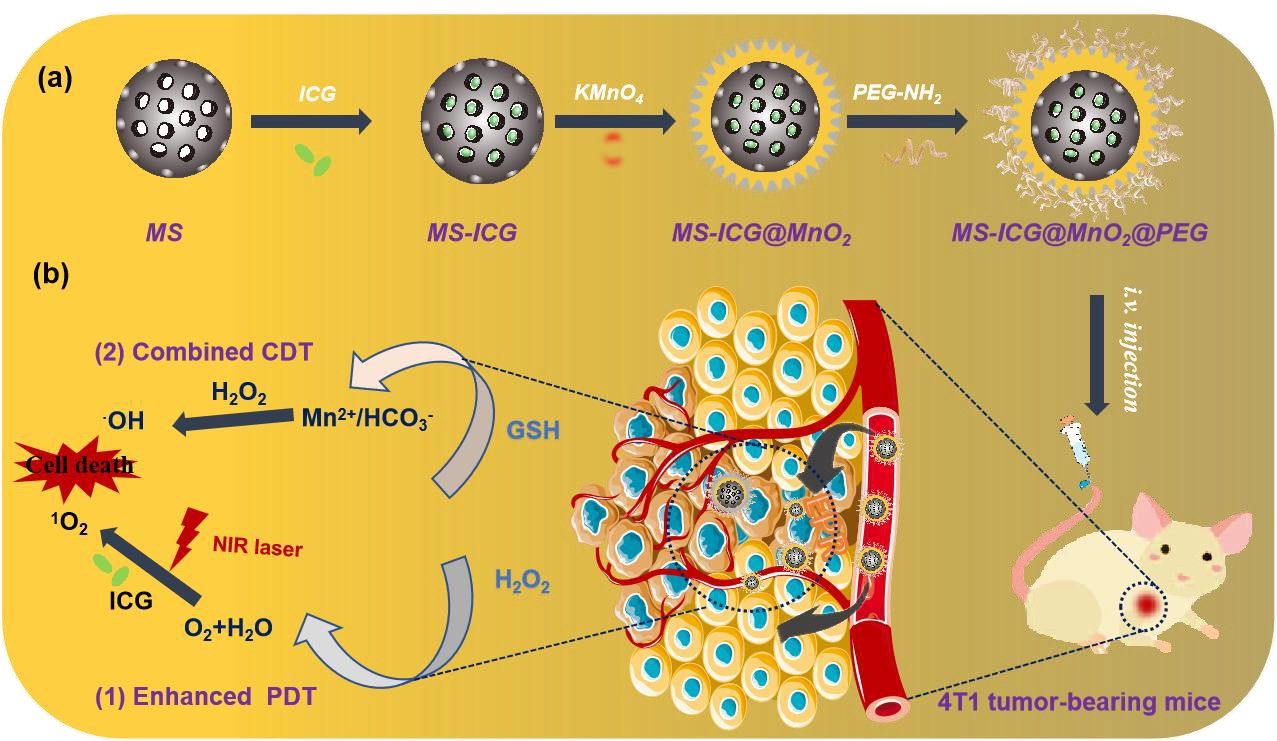
Xufeng Zhu. et al. In Situ Fabrication of MS@MnO2 Hybrid as Nanozymes for Enhancing ROS‐Mediated Breast Cancer Therapy. Nanoscale. 2020
DOI: 10.1039/D0NR03931D
https://pubs.rsc.org/en/content/articlelanding/2020/nr/d0nr03931d#!divAbstract



















