如何增强药物的血液循环稳定性和实效肿瘤特异性给药被认为是纳米医学(NMs)实现临床转化的关键挑战之一。川崎工业振兴研究所Sabina Quader和Kazunori Kataoka开发了一种超分子激活、肿瘤细胞内(Tex)pH触发的纳米结构,它可以在体循环中维持胶束结构,并通过感知肿瘤的异质性pH以在瘤内逐步释放药物。
本文要点:
(1)实验将抗癌药物长春花碱的衍生物去乙酰长春碱酰肼(DAVBNH)与脂肪族酮功能化的聚(乙二醇)b-聚(氨基酸)共聚物进行结合以构建了该聚合物胶束。实验结果表明,这种对Tex-pH敏感的DAVBNH胶束(Tex-micelle)在原位胶质瘤(GBM)模型中是有效和安全的。与游离的DAVBNH相比,该胶束可以使得移植型GBM肿瘤模型的中位生存期延长1.4倍,同基因GBM模型的中位生存期延长2.6倍。
(2)综上所述,这一研究工作为开发智能型NMs提供了新的分子设计策略,充分证明了利用对Tex-pH值的感知以开发临床相关的纳米技术平台有望在治疗恶性胶质瘤方面实现临床转化。
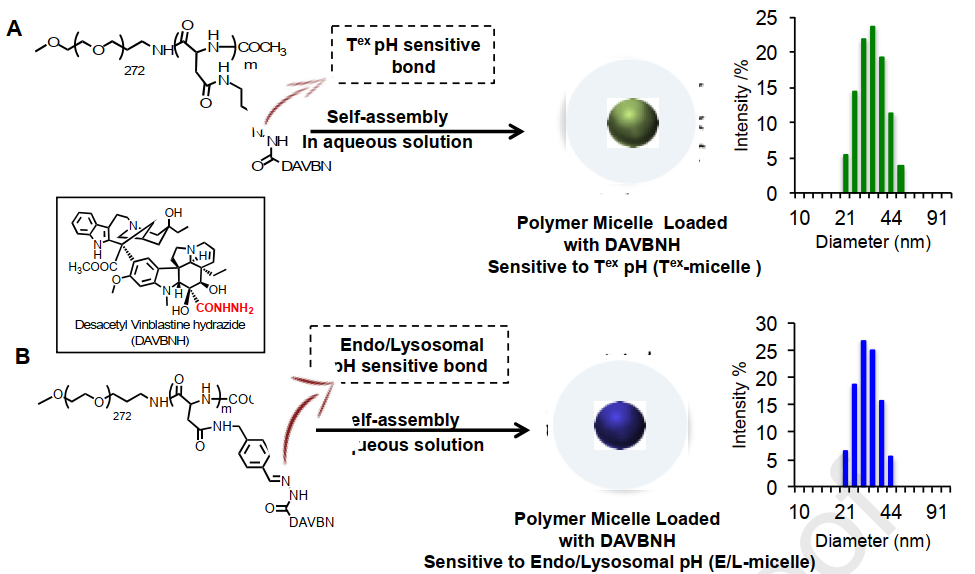
Sabina Quader. et al. Supramolecularly enabled pH- triggered drug action at tumor microenvironment potentiates nanomedicine efficacy against glioblastoma. Biomaterials. 2020
https://www.sciencedirect.com/science/article/pii/S0142961220307092



















