[FeFe]氢化酶是氢与质子和电子相互转化的有效催化剂,其催化机理一直存在争议。其活性中心H-簇由共价连接到[2Fe]亚簇([2Fe]H)的[4Fe−4S]亚簇([4Fe−4S]H)组成。研究表明,这两个亚团簇是强氧化还原偶联的,H-团簇内的质子耦合电子转移(PCET)被认为是催化活性所必需的。此外,还提出了基于[4Fe−4S]H的质子耦合还原反应。
近日,德国马克斯-普朗克能源转换研究所James A. Birrell,Patricia Rodríguez-Maciá报道了用两种不同的[FeFe]氢酶:来自莱茵衣藻(Chlamydomonas reinhardtii)的CrHydA1和来自巴氏梭菌(Clostridium pasteurianum)的CpHydA1,用红外光谱(IR)电化学研究了[4Fe-Fe4S]H氧化还原行为的pH依赖性。
文章要点
1)与以前的报道相反,研究发现,在该实验条件下,[4Fe−4S]H的氧化还原电位与pH无关,这两种酶的生理值都在附近。此外,研究人员还发现了[4Fe−4S]与CpHydA1中的辅助分子的[4Fe−4S]簇(F簇)之间的氧化还原反协同行为,从而调节了活性中心的催化作用。
2)结果表明,[FeFe]氢酶的催化循环可能不涉及[4Fe−4S]H或附近的质子化,而是有利于[2Fe]H质子化驱动催化的模型。
研究发现为[FeFe]氢酶的催化机理提供了新的线索,并强调了F-簇在微调催化中的重要性。
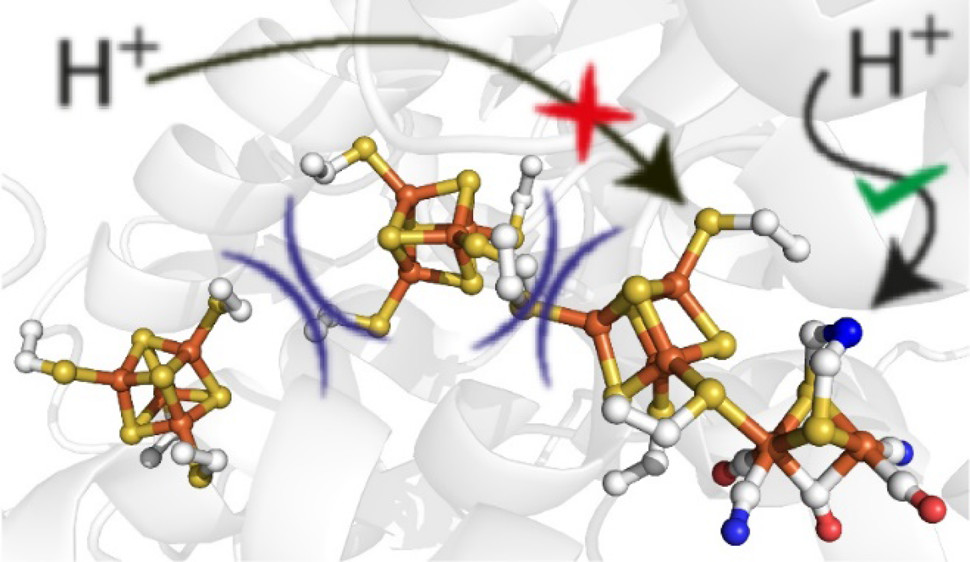
Patricia Rodríguez-Maciá, et al, Insight into the Redox Behavior of the [4Fe−4S] Subcluster in [FeFe] Hydrogenases, ACS Nano, 2020
DOI: 10.1021/acscatal.0c02771
https://dx.doi.org/10.1021/acscatal.0c02771



















