人血清白蛋白(HSA)具有生物相容性好、循环时间长的特点,被广泛用作难溶性抗癌药物的载体,但也存在肿瘤靶向性弱、药物释放不可控等缺点。在此,江南大学陈敬华、周娟等人通过基因融合技术在HSA分离端引入聚组氨酸 (pHis)、基质金属蛋白酶-2(MMP-2)消化和精氨酸-甘氨酸-天冬氨酸 (RGD)肽,以提高HSA的生物学性能。
本文要点:
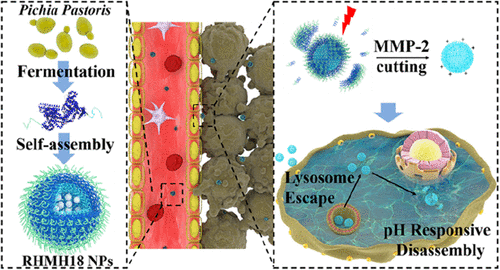
1)由毕赤酵母表达的蛋白在将疏水药物紫外光醇(PTX)装入聚组氨酸胶束核的同时,可以自组装成3RGD-HSA-MMP-18His纳米颗粒(RHMH18 NPs)。
2)RHMH18 NPs通过RGD介导的对肿瘤血管内皮上调的ανβ3-整联蛋白的特异性结合,可导致肿瘤部位治疗物质的富集,从而表现出高效的肿瘤靶向活性。
3)一旦到达肿瘤微环境,RHMH18 NPs被MMP-2切断,去除HSA-3RGD部分,只留下带正电荷的小组氨酸胶束,可以更有效地穿透肿瘤组织深部。最后,组氨酸胶束根据pH响应成功地从溶酶体中逃逸并释放药物。
4)体内实验结果表明,三级推进型RHMH18 NPs具有较好的肿瘤抑制活性,且副作用小,为肿瘤治疗提供了基于蛋白的药物递送系统的潜在策略。
Mingyu Wang, et al. Bioengineered Human Serum Albumin Fusion Protein as Target/Enzyme/pH Three-Stage Propulsive Drug Vehicle for Tumor Therapy. ACS Nano, 2020.
DOI: 10.1021/acsnano.0c07610
https://doi.org/10.1021/acsnano.0c07610


















