肽和蛋白质治疗剂的剂量因从血池中快速清除和差的细胞膜通透性而变得复杂。长期以来,人们一直探索将他们包封在纳米载体(如脂质体或多聚体)中来克服这些局限性,但是制造方面的挑战限制了这些方法的临床应用。近年来,已经开发了反向闪速纳米沉淀法(iFNP)以制备高负载的聚合物纳米载体,其中所述肽或蛋白质包含在亲水核内,并由疏水聚合物壳稳定。对具有高阶结构的蛋白质进行封装需要了解加工过程如何影响其构象状态。在此,美国普林斯顿大学Pablo G. Debenedetti、Robert K. Prud’homme等人以Trp-笼蛋白TC5b为模型,采用实验/模拟相结合的方法来表征iFNP加工过程中的蛋白质行为。
本文要点:
1)具有增强采样技术的显式溶剂全原子分子动力学模拟与二维异核多量子相干核磁共振波谱(2D-HMQC NMR)和圆二色性相结合,以确定在iFNP处理过程中遇到的混合溶剂暴露期间TC5b的结构。
2)模拟涉及混合溶剂和蛋白质的原子模型,以捕获水,二甲基亚砜(DMSO)和蛋白质之间氢键键合和疏水相互作用的复杂性。组合分析揭示了蛋白质在11 M DMSO中的结构展开,但证实了从聚合物纳米载体释放回到水相后的完全复性。
这些结果突出了模拟和NMR为蛋白质在纳米载体中的形成提供的见解。
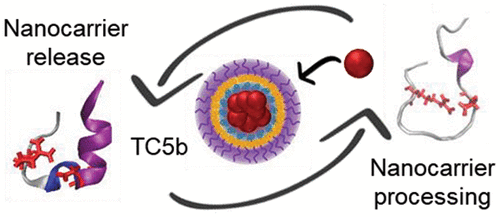
Chester E. Markwalter, et al. Stability of Protein Structure during Nanocarrier Encapsulation: Insights on Solvent Effects from Simulations and Spectroscopic Analysis, ACS Nano, 2020.
DOI: 10.1021/acsnano.0c06056
https://doi.org/10.1021/acsnano.0c06056


















