通过光动力治疗(PDT)将肿瘤相关巨噬细胞重编程为抗肿瘤的M1表型是克服肿瘤免疫抑制微环境和促进肿瘤免疫治疗的一种有效策略。但是目前,有关I型和II型机制产生的活性氧(ROS)与巨噬细胞的极化效应之间的关系尚不清楚。南方科技大学李凯研究员设计和合成了三种具有聚集增强ROS生成的供体-受体结构光敏剂,它们的ROS生成效率可以通过改变受体来调节,从而产生不同的活化巨噬细胞的能力。
本文要点:
(1)实验发现I型机制产生的细胞外ROS主要负责将巨噬细胞从M2型重编程为抗肿瘤的M1表型。体内实验进一步证明,AIEgen光敏剂可触发光动力-免疫治疗,有效抑制小鼠肿瘤生长,而其在巨噬细胞减少的小鼠模型中的治疗效果则明显不佳。
(2)综上所述,这一研究为设计可以激活巨噬细胞的光敏剂分子提供了参考指南,并为理解巨噬细胞活化在光动力-免疫治疗过程中的工作原理提供了新的见解。
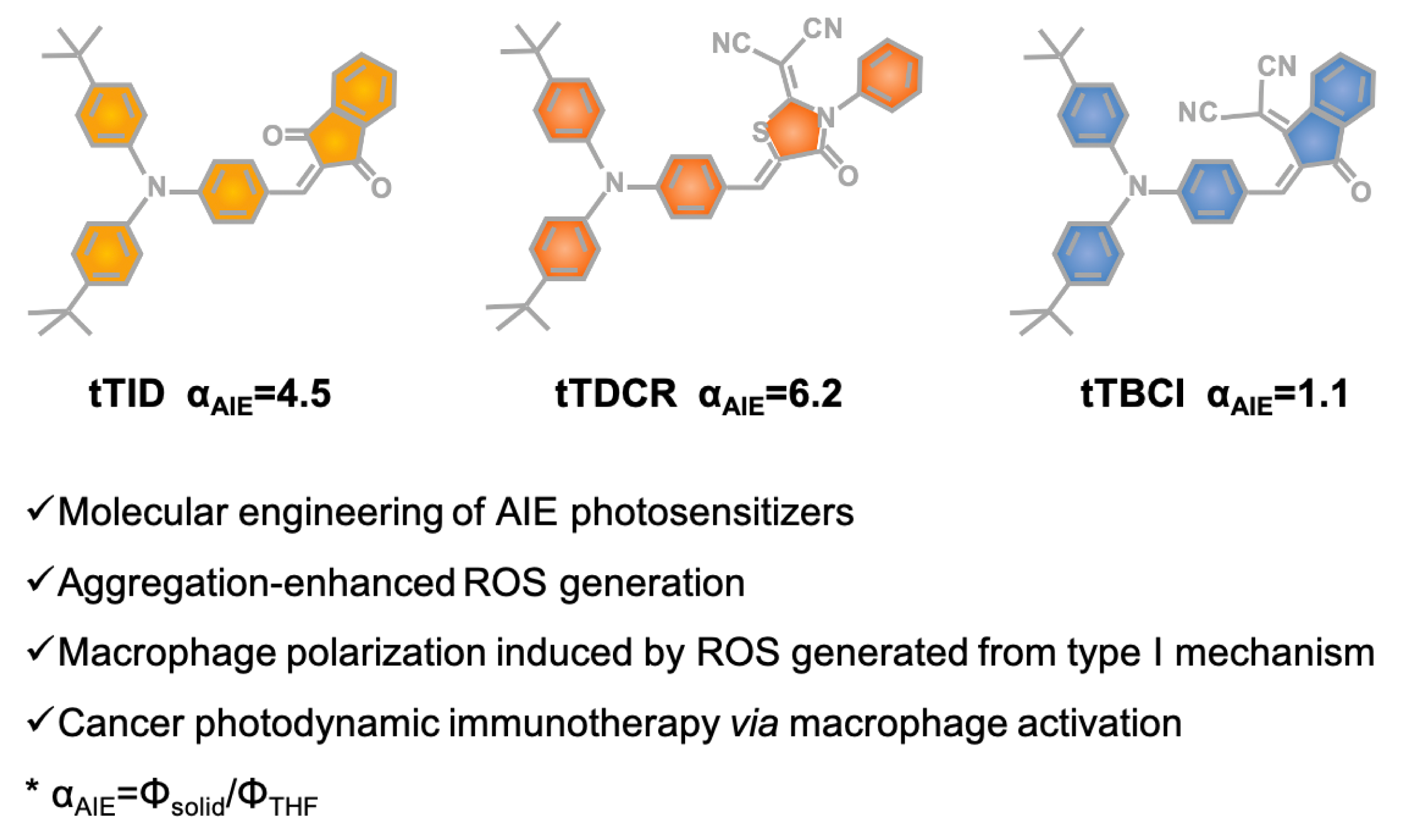
Guang Yang. et al. Acceptor Engineering for Optimized ROS Generation Facilitates Reprogramming Macrophages to M1 Phenotype in Photodynamic Immunotherapy. Angewandte Chemie International Edition. 2020
DOI: 10.1002/anie.202013228
https://onlinelibrary.wiley.com/doi/10.1002/anie.202013228



















