免疫疗法已经彻底改变了癌症治疗。然而,只有少数患者对目前可用的免疫治疗方案有反应。在此,中国医学科学院北京协和医学院王伟伟、Yumin Zhang,天津大学董岸杰等人证明RNA干扰(RNAi)结合免疫原性化疗可以引发针对黑色素瘤的有效抗肿瘤免疫力。
本文要点:
1)开发了阳离子聚合物-脂质杂化纳米囊泡(P/LNVs),作为阿霉素和小干扰RNA(siRNA)的新型递送系统,对B16细胞具有广泛的细胞毒性和基因沉默效率。
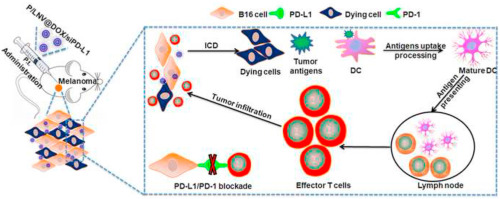
2)负载阿霉素的P / LNVs通过聚(ADP-核糖)聚合酶1依赖性(PARP1)凋亡途径诱导B16细胞的免疫原性细胞死亡而直接原位增加了内源性肿瘤抗原的表达和呈递,从而在小鼠体内产生了显著的抗肿瘤免疫应答。
3)利用垂死的B16细胞作为疫苗接种策略,结合基于RNAi的程序性细胞死亡配体1(PD-L1)的敲除,在预防和转移性黑色素瘤方面均显示出功效。值得注意的是,与亚治疗剂量的阿霉素协同作用的PD-L1阻滞引发了强大的治疗性抗肿瘤T细胞反应,并在30%患有B16黑色素瘤的小鼠中根除了预先建立的肿瘤。
4)研究表明,这种联合治疗提供了一种新的强大的免疫治疗方式,其特点是效应CD8+ T细胞的浸润显著增加,并有效缓解了肿瘤中免疫抑制性微环境。P/LNV是一种多功能且高度可扩展的载体,可以实现纳米医学和RNAi的广泛结合,为晚期癌症提供新的治疗策略。
Changrong Wang, et al. Polymer-lipid hybrid nanovesicle-enabled combination of immunogenic chemotherapy and RNAi-mediated PD-L1 knockdown elicits antitumor immunity against melanoma. Biomaterials, 2020.
DOI: https://doi.org/10.1016/j.biomaterials.2020.120579
https://doi.org/10.1016/j.biomaterials.2020.120579


















