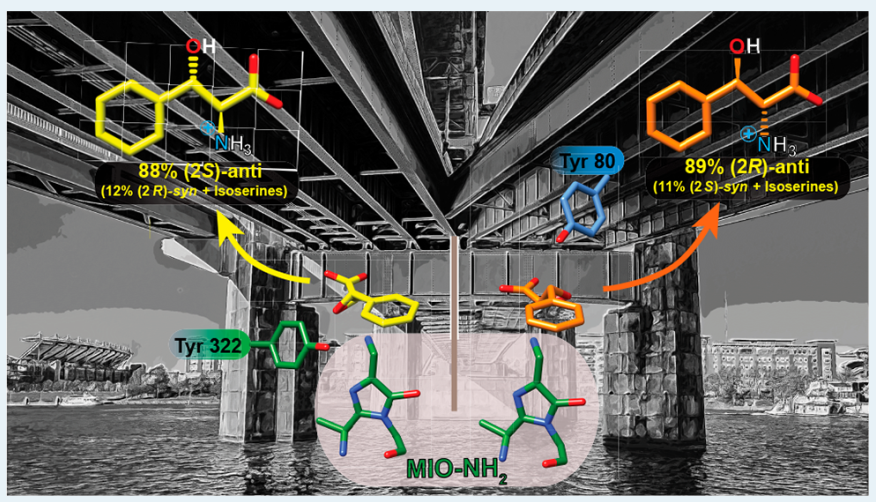
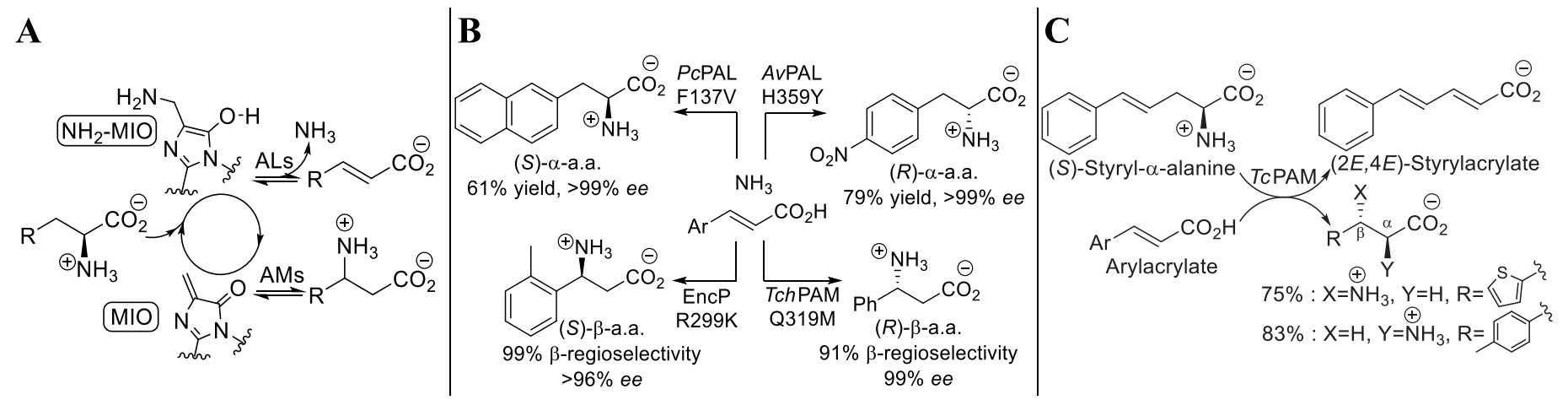
β-羟基-α-氨基酸是一种非常规结构氨基酸,含有两个立体结构中心位点,在药物化学、农药化学领域有着重要应用,有鉴于此,密歇根州立大学Kevin D. Walker等报道了一种从TcPAM(加拿大红豆杉,Taxus canadensis)氨基变位酶出发的5-叉甲基-3,5-二氢-4H-咪唑-4-酮,从(S)-苯乙烯-α-丙氨酸转化为3-苯甘氨酸酯,从而产生抗苯基丝氨酸的立体选择性。
本文要点:
(1)
通过TcPAM作为催化剂,通过位点选择性的将Cβ位点的胺基转化,导致选择性生成苯丝氨酸(phenylserine),选择性达到97 %。与此同时,苯异丝氨酸的选择性仅仅为3 %。
(2)
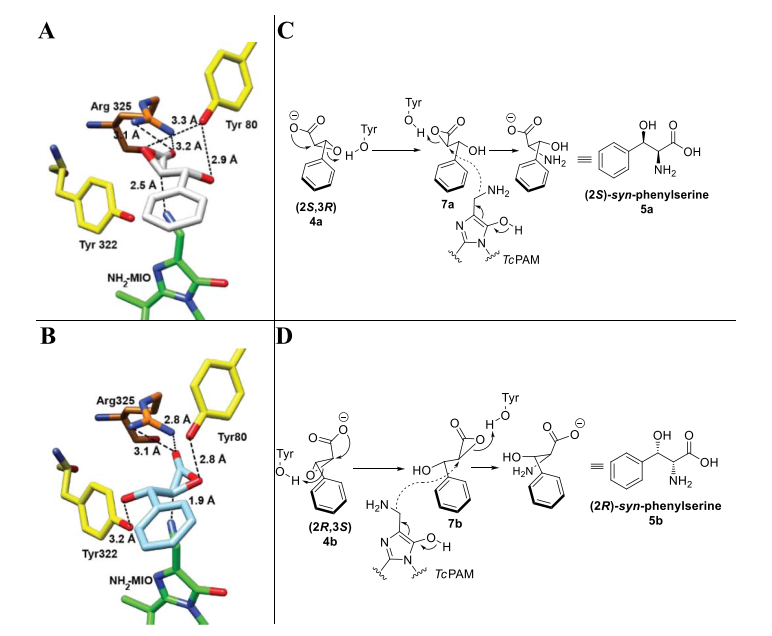
气相色谱-质谱分析这种酶催化反应的结果显示,对每种glycidate对映体都实现了立体选择性的胺基转移。TcPAM将(2S,3R)- 3-苯基缩水甘油酸转化为(2S)-anti-苯丝氨酸,选择性达到89 %;将(2R,3S)-anti-苯基缩水甘油酸选择性的转化为(2R)-anti-苯丝氨酸,选择性达到88 %。在两个反应中,在Cα位点上都产生了构象转变。两种对映体苯基缩水甘油酸在反应过程中都产生了少量(~10 %)syn-苯丝氨酸用于保持Cα位点的构象。
(3)
TcPAM对(2S,3R)- 3-苯基缩水甘油酸有微弱的选择性,对(2S,3R)- 3-苯基缩水甘油酸的反应速率常数(0.3 min-1)比(2S,3R)-结构分子的反应速率常数(0.2 min-1)更高。这种对反应动力学的结果展示了苯基缩水甘油酸胺基化反应中对底物的ping-pong机理。
参考文献
Prakash K. Shee, Honggao Yan, and Kevin D. Walker*, Intermolecular Amine Transfer to Enantioenriched trans-3-Phenylglycidates by an α/β-Aminomutase to Access Both antiPhenylserine Isomers, ACS Catal. 2020, 10, 15071−15082
DOI: 10.1021/acscatal.0c03977
https://pubs.acs.org/doi/10.1021/acscatal.0c03977





















