为了提高光热/光动力协同疗法(PTT/PDT)对缺氧性肿瘤的治疗效果,西安交通大学吴道澄等人战略性地开发了一种具有深层穿透性和pH响应性的复合纳米系统。
本文要点:
1)通过将血红蛋白(Hb)和二氢卟酚e6共载于聚多巴胺上以构建小尺寸PHC NPs,从而构建了纳米系统--[PHC]PP@HA NPs,将其封装在聚合物胶束聚乙二醇–聚乙烯亚胺中,然后用功能化的透明质酸端封。
2)pH响应特性使[PHC]PP@HA NPs在血液循环中保留了140 nm的初始大小,但在肿瘤微环境中迅速释放了小的PHC NPs(〜10 nm),具有较高的肿瘤穿透能力。体外穿透实验结果表明,PHC NPs在多细胞肿瘤球体中的穿透深度超过110μm。
3)[PHC]PP@HA NPs在缺氧条件下表现出优异的生物相容性,肿瘤深部通透性,高光热转化效率(47.09%)和低结合指数(0.59)。
4)值得注意的是,纳米系统基于肿瘤活性的反馈,可按需自由调节氧气的释放并破坏PHC NPs。这种反馈肿瘤疗法显著改善了PTT/PDT的协同作用,并降低了其毒副作用。体内抗肿瘤结果表明,按需供氧的[PHC]PP@HA NPs的抑瘤率约为100%,比单独使用PTT和不含Hb的纳米颗粒([PC]PP@HA NPs)好得多。
5)由反馈肿瘤治疗指导的[PHC]PP@HA NPs介导的PTT/PDT在60 天后实现了有效的消融,肿瘤复发率极低(8.3%),表明其用于PTT/PDT具有广泛的潜力。
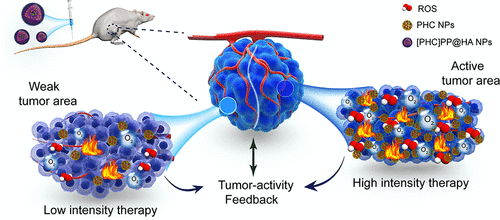
Ya Wang, et al. Highly Penetrable and On-Demand Oxygen Release with Tumor Activity Composite Nanosystem for Photothermal/Photodynamic Synergetic Therapy. ACS Nano, 2020.
DOI: 10.1021/acsnano.0c06415
https://doi.org/10.1021/acsnano.0c06415


















