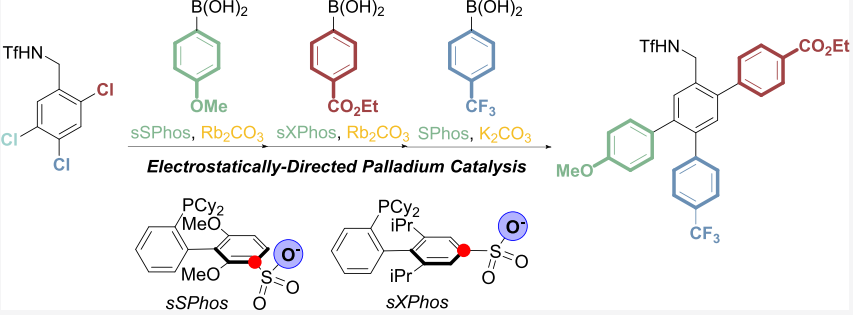
通过配体和底物之间的非共价相互作用,在调控反应的位点选择性中受到了越来越多关注,其中关键点在于通过对静电相互作用对相互靠近的不同反应位点实现选择性的控制。有鉴于此,剑桥大学Robert J. Phipps等报道了一套催化剂体系(由2个紧密联系的磺化膦配体和5种不同阳离子半径的碱相互配合),实现了对多氯芳烃进行位点选择性的Suzuki-Miyaura、Buchwald-Hartwig偶联。本工作展示了一种位点选择性交叉偶联反应合成复杂、多取代芳烃的方法学。
本文要点:
(1)
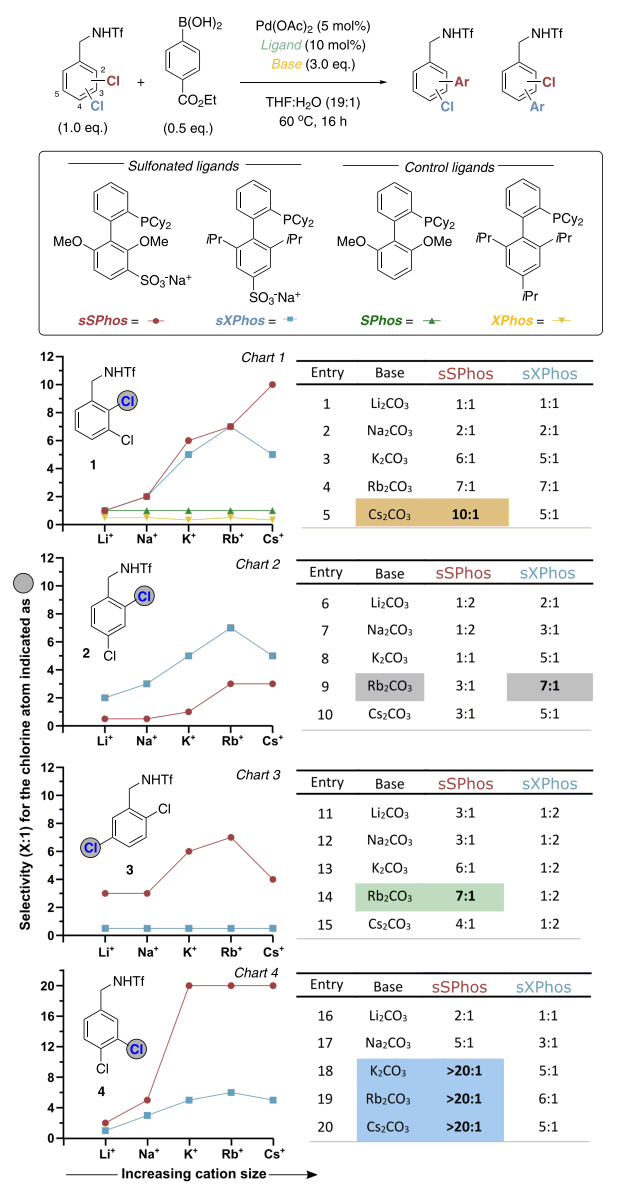
反应优化。以多氯苯甲胺基三氟甲磺酰(1)、对甲酸乙酯苯硼酸作为反应物,在5 mol % Pd(OAc)2作为过渡金属催化剂种的偶联反应,在THF/H2O (19:1)混合溶剂种于60 ℃种反应。通过改变配体、碳酸类碱的阳离子(Li, Na, K, Rb, Cs),优化多氯芳烃偶联反应产率。
(2)
在2,3-二氯苯甲胺基三氟甲磺酰(1)的反应中,发现碱选择Cs2CO3、配体为sSPhos,对C2上的氯有较好的选择性(10:1);在2,4-二氯苯甲胺基三氟甲磺酰(2)的反应中,发现碱选择Pb2CO3、配体为sXPhos,对C2上的氯有比较好的选择性(7:1);在2,5-二氯苯甲胺基三氟甲磺酰(3)的反应中,发现碱选择Rb2CO3、配体为sSPhos,对C5上的氯有比较好的选择性(7:1);在3,4-二氯苯甲胺基三氟甲磺酰(4)的反应中,发现碱选择K2CO3或Rb2CO3或Cs2CO3、配体选择sSPhos,对C3上的氯有比较好的选择性(>20:1)。
(3)
通过对大量底物反应性的总结和考察,展示了通过精确调节配体/碱的组合情况,从而实现对反应选择性的控制。位于间位的氯首先进行偶联反应,此时当邻位没有氯,更容易和催化剂结合发生偶联反应;邻位氯原子的反应性弱于间位氯原子;对位氯原子、邻位氯原子修饰的间位氯有最弱的反应性。
配体中的磺酸根取代基对反应产生选择性极为重要,但是特定选择性需要通过对磺酸基的位置、碱的阳离子进行筛选。在目前的反应中,难以进行预测配体、碱的物种用于实现较好的选择性,仍需要实验进行筛选。
参考文献
William A. Golding, Hendrik L. Schmitt, and Robert J. Phipps*, Systematic Variation of Ligand and Cation Parameters Enables SiteSelective C-C and C-N Cross-Coupling of Multiply Chlorinated Arenes through Substrate-Ligand Electrostatic Interactions, J. Am. Chem. Soc. 2020
DOI: 10.1021/jacs.0c11056
https://pubs.acs.org/doi/10.1021/jacs.0c11056




















