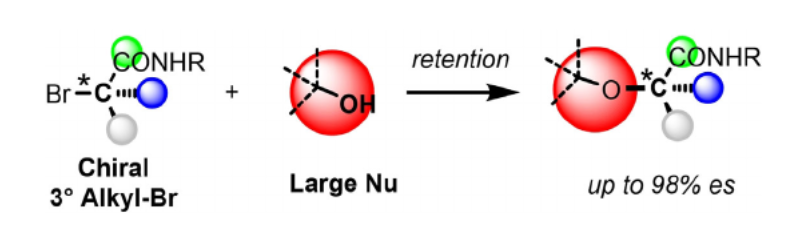
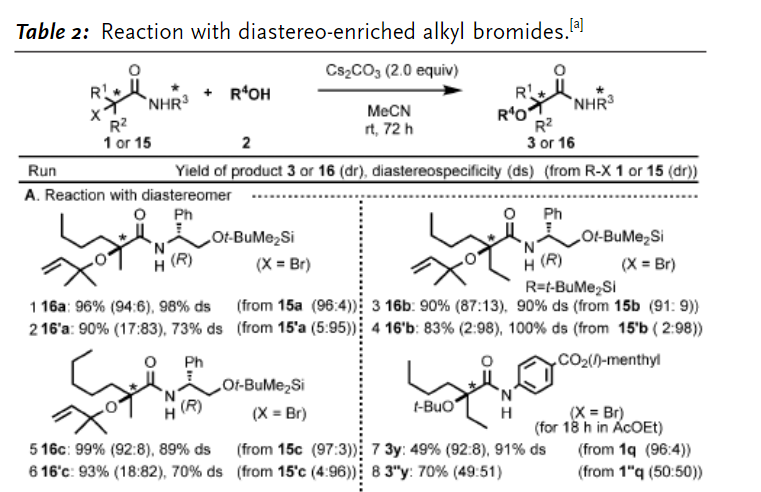
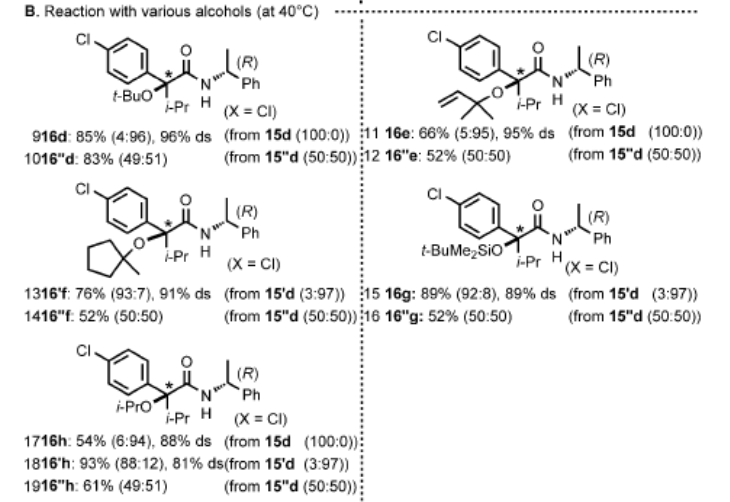
SN1、SN2等亲核取代反应时经典可靠的反应,但是这种反应中对大体积亲核试剂、手性三级烷亲电试剂合成手性四级碳中心的反应中较为困难。通过自由基物种的SRN1反应是另外一种传统方法用于对大体积亲核试剂、烷基卤化物进行亲核取代反应的方法,但是该反应方法学不兼容三级碳烷基亲电试剂。因此,对于通过手性三级烷基亲电试剂核大体积亲核试剂之间的立体结构定向亲核取代反应没有很好的结果。有鉴于此,日本山口大学Takashi Nishikata、鸟取大学Toshiki Nokami、东京工业大学Takashi Koike、广岛大学Manabu Abe等报道了通过三级烷基醇、手性/非手性α-溴羧酰胺进行合成立体拥挤的醚分子,构建了含有立体定向的两个不同三级烷基醚产物。
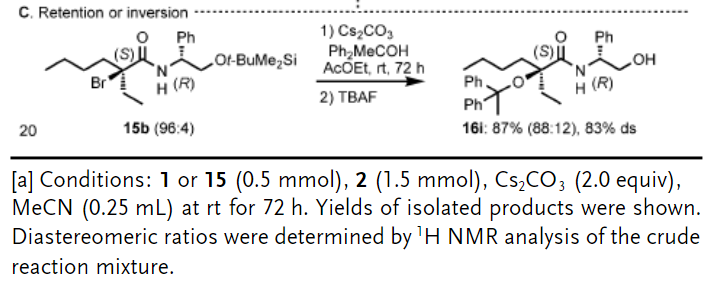
参考文献
Dr. Goki Hirata, Kentarou Takeuchi, Yusuke Shimoharai, Prof. Dr. Michinori Sumimoto, Hazuki Kaizawa, Prof. Dr. Toshiki Nokami*, Prof. Dr. Takashi Koike*, Prof. Dr. Manabu Abe*, Prof. Dr. Eiji Shirakawa*, Prof. Dr. Takashi Nishikata*, Chemistry of Tertiary Carbon Center in the Formation of Congested C−O Ether Bonds, Angew. Chem. Int. Ed. 2020,
DOI: 10.1002/anie.202010697
https://www.onlinelibrary.wiley.com/doi/full/10.1002/anie.202010697


















