被活化的血小板可以维持肿瘤血管的完整性,从而导致肿瘤灌注受限,并使得纳米颗粒类药物的抗肿瘤疗效欠佳。为了通过抑制血小板的活化以破坏肿瘤血管内皮屏障,复旦大学张奇志教授和上海大学Yan Wei构建了一种载丹参酮IIA(TNA)的TM33肽修饰的明胶/油酸纳米颗粒(TM33-GON/TNA)。
本文要点:
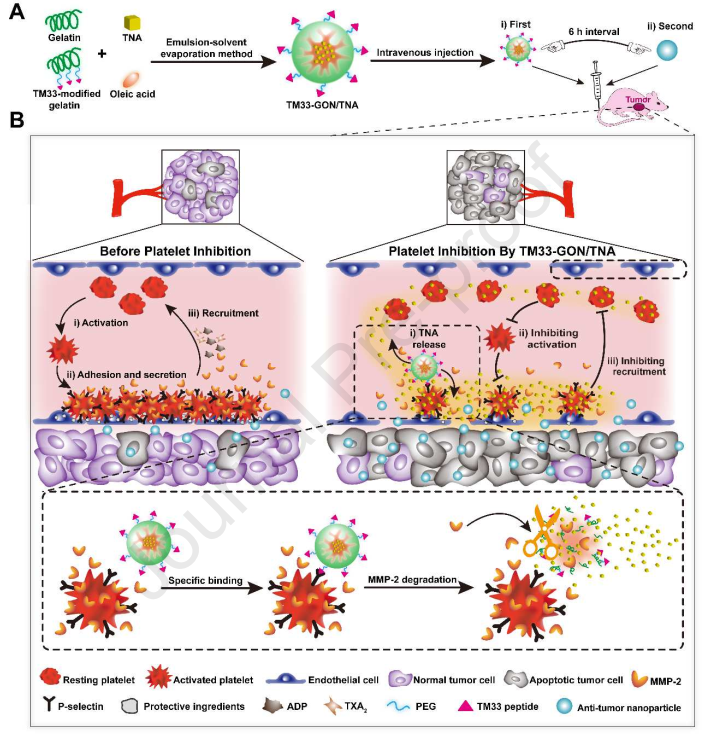
(1)TM33-GON/TNA在基质金属蛋白酶2(MMP-2)刺激下可通过特异性结合P-选择素而粘附到被活化的血小板上,并将TNA释放到细胞外空间,导致产生局部高水平的TNA。因此,在被激活的血小板周围的局部环境中所发生的血小板活化、粘附和聚集均会被有效地抑制,从而导致肿瘤内皮连接发生渗漏。
(2)因此,经TM33-GON/TNA治疗后,伊文思蓝(大分子标记物)、小尺寸Nab-PTX(~10 nm)和大尺寸DOX-Lip(~100 nm)的肿瘤渗透性分别增加了3.2倍、4.0倍和11.2倍,而它们对正常组织的药物递送量则没有增加。实验也在小鼠胰腺癌模型中证明了TM33-GON/TNA与Nab-PTX相联合可以表现出卓越的抗肿瘤疗效和很低的副作用。此外,由于血小板数量没有减少,TM33-GON/TNA所破坏的内皮连接可在治疗后实现可逆的恢复,进而降低不良的系统性出血风险。综上所述,TM33-GON/TNA有望作为一种具有临床转化前景的辅助治疗方式,以增强现有纳米药物在胰腺癌和其他肿瘤中的抗肿瘤疗效。
Jinxu Cao. et al. ‘Adhesion and Release’ Nanoparticle-Mediated Efficient Inhibition of Platelet Activation Disrupts Endothelial Barriers for Enhanced Drug Delivery in Tumors. Biomaterials. 2020
https://www.sciencedirect.com/science/article/pii/S014296122030867X



















