磷酸化是最常见的可逆蛋白质翻译后修饰(PTM)。由于给定激酶经常在细胞中有许多底物、参与多种功能,传统酶的抑制会产生意外的结果。有鉴于此,美国爱荷华州立大学的Yan Zhao等研究人员,通过选择性抑制多肽底物实现激酶活性的控制。
本文要点
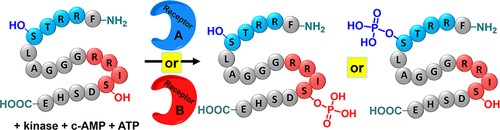
1)研究组报告合成受体首次用于精确操纵激酶磷酸化,利用受体高亲和性及高特异性结合肽段的能力。
2)抑制使得选择性磷酸化混合物中具有同样共有模体的肽段成为可能。一个特定磷酸化位点可以被抑制,同时相同底物的其他位点可以进行磷酸化。
3)这些受体可能独立作用于他们定向的链,或者参与保护一段长序列的片段。
4)源自结合的抑制作用能够与多域激酶内的蛋白质相互作用竞争,从而使受控的PTM能够以前所未有的方式进行。
参考文献:
Xiaowei Li, et al. Controlling Kinase Activities by Selective Inhibition of Peptide Substrates. JACS, 2020.
DOI:10.1021/jacs.0c11566
https://pubs.acs.org/doi/10.1021/jacs.0c11566


















