对索拉非尼的耐药性严重阻碍了其对肝细胞癌(HCC)的有效性。癌症干性与索拉非尼的耐药性密切相关。逆转癌症干性的方法仍然是研究中最大的关注之一,缺乏此类方法阻碍了目前的HCC治疗。据报道,泛素特异性蛋白酶22(USP22)在HCC干性和多药耐药性(MDR)中起着关键作用。在此,浙江大学徐骁、Jiajia Xiang等人利用半乳糖修饰的脂质多聚体(Gal-SLP)开发了一种靶向HCC的自激活级联反应纳米平台,可共同递送索拉非尼和USP22 shRNA(shUSP22)用于协同HCC治疗。
本文要点:
1)包裹在Gal-SLPs中的索拉非尼诱导活性氧(ROS)级联反应并触发shUSP22快速释放。因此,Gal-SLPs极大地抑制了USP22的表达。
2)USP22的下调抑制多药耐药相关蛋白1(MRP1),诱导细胞内索拉非尼积累,并阻碍HCC细胞的糖酵解。结果,Gal-SLPs有效抑制了HCC细胞的存活、增殖和集落形成。
3)建立了对索拉非尼不敏感的患者源异种移植(PDX)模型,并将其用于评估Gal-SLPs的体内抗肿瘤作用。 Gal-SLPs具有强大的抗肿瘤功效和生物安全性。因此,Gal-SLPs有望在HCC的临床治疗中发挥巨大的潜力。
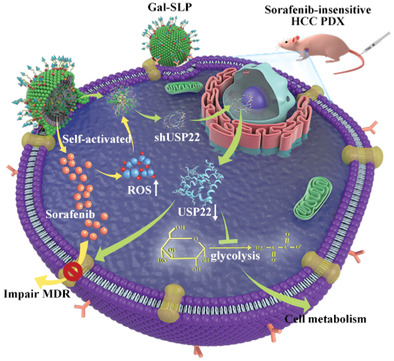
Shengjun Xu, et al. Self‐Activated Cascade‐Responsive Sorafenib and USP22 shRNA Co‐Delivery System for Synergetic Hepatocellular Carcinoma Therapy, Adv. Sci., 2021.
DOI: 10.1002/advs.202003042
https://doi.org/10.1002/advs.202003042


















