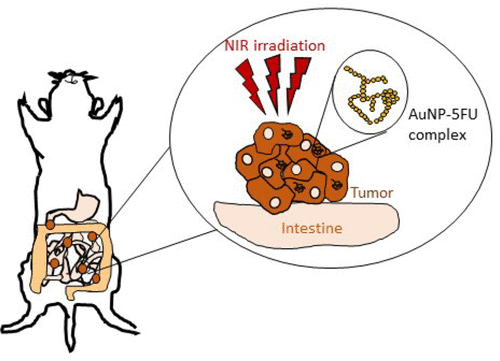
腹膜转移(PM)被认为是转移性结肠癌的晚期期,即使采用最新最好的化疗方案,其中位生存率仍较低。目前的PM治疗结合了细胞减灭手术(包括切除所有肉眼可见的肿瘤)和腹腔热化疗(HIPEC),后者利用温热促进化疗药物的扩散和细胞毒作用。由于HIPEC是通过含有化疗的热液体的封闭循环进行的,它会导致不受控制的加热和药物在整个腹腔内的分布,具有重要的场外毒性和高的发病率。有鉴于此,法国巴黎大学Florence Gazeau等人提出了一种更安全的精准策略,使用近红外(NIR)光激活金纳米粒子(AuNPs)耦合化疗药物5-氟尿嘧啶(5-FU),以实现靶向腹腔内肿瘤结节温和化疗热疗的空间和时间控制。
本文要点:
1)16 nm AuNPs及其与5-FU复合物(AuNP-5-FU)在皮下结肠肿瘤微环境和同基因小鼠的PM中均被证明是有效的近红外光热剂。
2)值得注意的是,5-FU参与的近红外光热疗法提供了额外的抗肿瘤效果。
3)单次腹腔注射AuNP-5-FU可导致其优先积聚在肿瘤结节和腹腔巨噬细胞中,允许光诱导选择性热疗,延长肿瘤坏死,激活促炎免疫反应,同时不损伤健康组织。
4)从转化角度来看,由AuNP -药物复合物介导的联合光热和肿瘤靶向化疗有可能在临床实践中克服HIPEC目前的非靶向毒性。
Vladimir Mulens-Arias, et al. Tumor-Selective Immune-Active Mild Hyperthermia Associated with Chemotherapy in Colon Peritoneal Metastasis by Photoactivation of Fluorouracil–Gold Nanoparticle Complexes. ACS Nano, 2021.
DOI: 10.1021/acsnano.0c10276
https://doi.org/10.1021/acsnano.0c10276


















