肿瘤微环境是由肿瘤细胞、免疫细胞和血管组成的复杂的多细胞系统。其中,血管是药物穿透组织的障碍之一。因此,实现对癌症的进行有效治疗就需要开发药物递送系统以克服存在于肿瘤微环境(TMEs)中的生物屏障。华盛顿州立大学王振家教授设计了一种基于细菌(大肠杆菌)双层膜衍生的纳米囊泡(DMVs),表达RGD多肽和内源性细菌靶向配体的药物递送系统。
本文要点:
(1)实验首先对DMVs的物理和生物学特性进行了表征,并通过pH梯度驱动的载药方法将阿霉素(DOX)载入DMVs中,并在小鼠黑素瘤移植模型中对负载DOX的DMVs的治疗效果进行了研究。体内外实验结果表明,DMVs可以靶向中性粒细胞和单核细胞,而这些中性粒细胞和单核细胞可以介导DMVs穿过血管屏障。并且,它们也可以直接靶向肿瘤血管系统和肿瘤细胞,从而实现在TMEs中进行治疗药物递送。
(2)此外,实验也开发了一种远程载药方法以有效地将DOX封装在DMVs中,其载药量为12% (w/w)。在B16-F10黑色素瘤小鼠模型中,实验发现DOX-RGD-DMVs可以明显地抑制肿瘤生长。综上所述,这一研究表明DMVs是一种可以在TMEs中同时靶向多种细胞,从而增强药物递送和改善癌症治疗的强大平台。
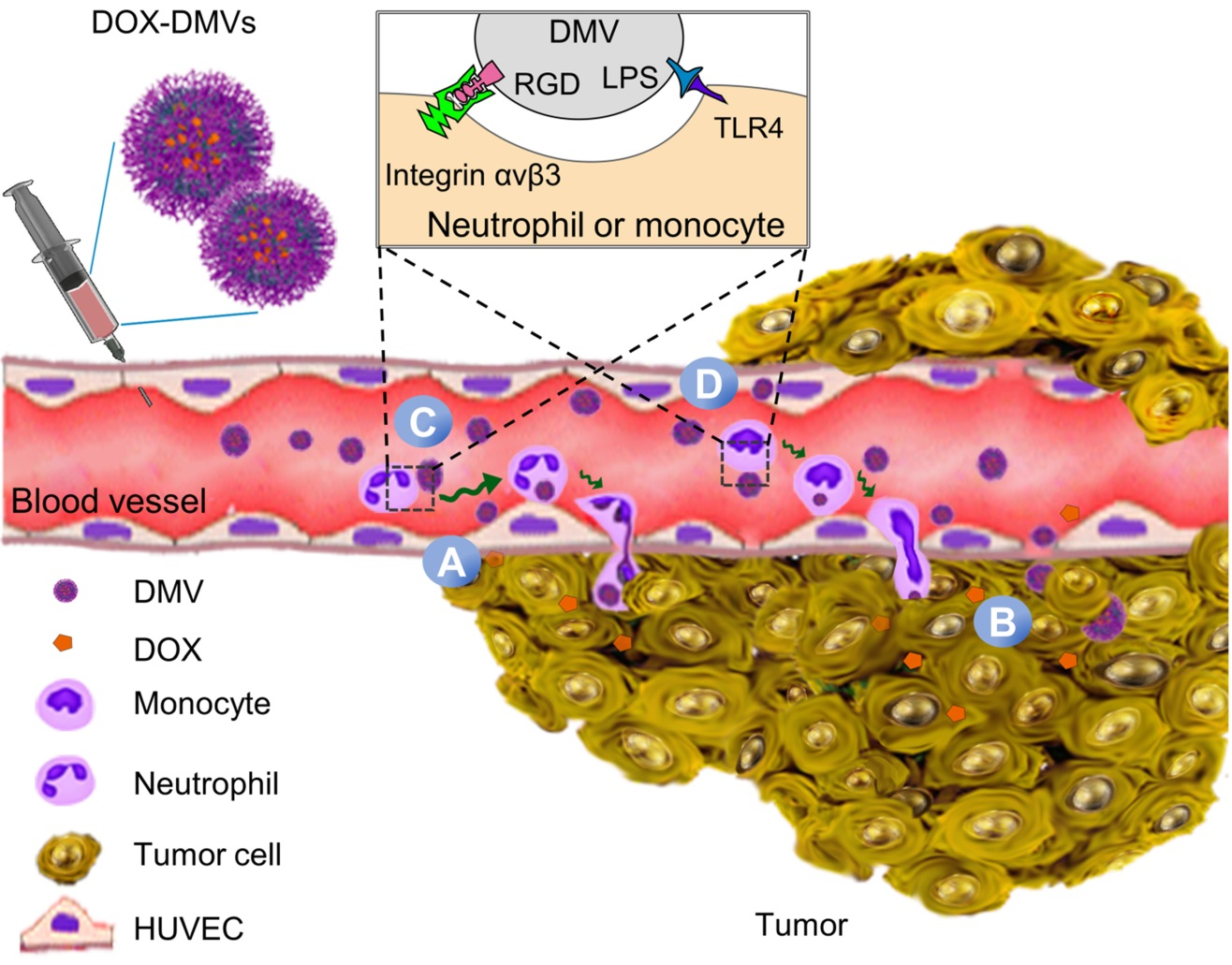
Jin Gao. et al. RGD-expressed bacterial membrane-derived nanovesicles enhance cancer therapy via multiple tumorous targeting. Theranostics. 2021
DOI: 10.7150/thno.51988
https://www.thno.org/v11p3301.htm



















