由于复杂的生物屏障,纳米粒子给药面临着靶向给药不精确和药物生物利用度低等挑战。在此,美国德克萨斯大学奥斯汀分校Nicholas A. Peppas、四川大学高会乐等人设计了级联靶向、双载药的核壳纳米颗粒(DLTPT),由靶向CD44的透明质酸修饰的阿霉素(HA-DOX)壳和靶向线粒体的三苯基膦衍生物的纳米颗粒核负载氯尼达明(LND)二聚体(LTPT)。
本文要点:
1)由于肿瘤归巢效应和负电荷透明质酸的作用,DLTPT表现出血液循环时间延长,并在肿瘤部位有效积累的特征。
2)随后HA-DOX外壳被胞外透明质酸酶降解,粒径变小,导致负电荷向正电荷转变,增加了肿瘤的渗透和内化。
3)HA-DOX的降解进一步加速了DOX的释放,并暴露带正电荷的LTPT核心,以实现LND快速内体逃逸和线粒体靶向递送。
4)值得注意的是,当DLTPT与抗PD - L1联合使用时,肿瘤生长受到抑制,从而诱导了对肿瘤转移的免疫应答。
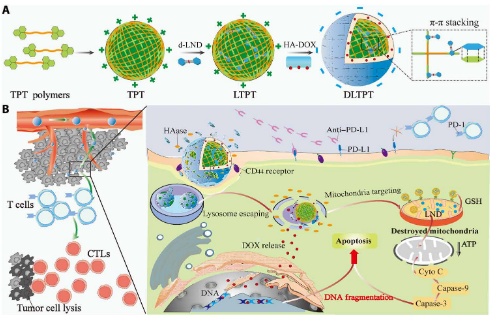
Yanmei He, et al. A combinational chemo-immune therapy using an enzyme-sensitive nanoplatform for dual-drug delivery to specific sites by cascade targeting. Sci. Adv., 2021.
DOI: 10.1126/sciadv.aba0776
https://advances.sciencemag.org/content/7/6/eaba0776


















