探索内源性分子概况对于理解细胞的功能和过程具有重要意义。尽管基于核酸的可编程适配体传感器在生物分子检测领域具有广阔的应用前景,但实现细胞内检测的靶向响应适配体传感器却很少实现,目前仍然存在一些挑战,包括基于淬灭的强度信号的量化/标准化的困难,探针结构的稳定性问题,以及通常需要广泛的结构建模的复杂传感器操作。有鉴于此,英国伦敦帝国学院Molly M. Stevens等人提出了一种具有仿生结晶自组装能力的肿瘤靶向DNA -无机杂化纳米复合适配体传感器,该传感器能够基于Förster共振能量转移(FRET)对胞内目标物丰度的变化进行定量解释。
本文要点:
1)利用滚环扩增技术驱动DNA纳米结构的设计可编程性和高通量制造,此设计平台提供了一种从多功能编码模板,包括细胞靶向适配体、比率型适配体传感器和胆固醇修饰元素,中自组装成稳定的纳米传感器的方法。
2)以前列腺癌细胞和细胞内三磷酸腺苷分子为模型体系,论证了胆固醇和适配体靶向递送的协同作用,以及定量细胞内适配体的可行性。
3)可以预见,这种方法提供了一种跨广泛目标系统的高度通用性的策略,用于生物可交付的纳米传感器的制备,以实现对内源性生物分子丰度的定量检测。
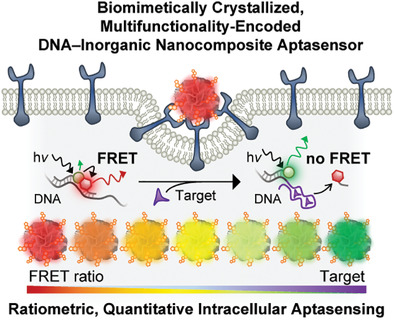
Nayoung Kim, et al. Tumor‐Targeting Cholesterol‐Decorated DNA Nanoflowers for Intracellular Ratiometric Aptasensing. Adv. Mater., 2021.
DOI: 10.1002/adma.202007738
https://doi.org/10.1002/adma.202007738


















