许多药物的疗效会受到其自身不良性质的影响,如较差的水溶性,低生物利用度和在体内的脱靶作用等。为了克服这些缺陷,人们研究开发了多种药物载体以增强治疗药物的药理特性。受光药理学所具有的高时空控制能力的启发,伦敦帝国学院James E. M. Lewis和Ramon Vilar利用机械保护作用将DNA靶向的金属药物笼化在可光降解的轮烷中。
本文要点:
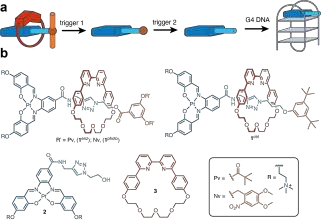
(1)实验所合成的轮烷它包含一个G-四联体DNA结合物,即PtII-salphen复合物,它可作为封闭单元。当这种化合物是机械联锁组合物的一部分时,它就不能与DNA发生相互作用。该轮烷中的第二个封闭子可在光或活性酯酶的作用下裂解。研究表明,在这些刺激因子的作用下,轮烷会分解以释放出PtII-salphen复合体并激活其与DNA结合的能力。
(2)实验还发现,与游离药物相比,该机械联锁系统在骨肉瘤细胞内的细胞通透性更增,而细胞毒性则很低。然而,光激活则会导致其细胞毒性急剧增加,这是由于其转位到细胞核和随后与DNA结合所引起的。
Timothy Kench. et al. Rotaxanes as cages to control DNA binding, cytotoxicity and cellular uptake of a small molecule. Angewandte Chemie International Edition. 2021
DOI: 10.1002/anie.202100151
https://onlinelibrary.wiley.com/doi/10.1002/anie.202100151



















