STING(干扰素基因刺激蛋白)是先天免疫的关键调节器,近年来被认为是一个很有前景的药物靶标。STING被环二核苷酸(CDNs)激活,最终导致I型干扰素和其他细胞因子的表达。迄今为止,人们对决定各种CDN类似物亲和力的因素知之甚少。有鉴于此,捷克科学院有机化学和生物化学研究所的Lubomir Rulisek等研究人员,发现配体分子的张力及其构象的复杂性是决定环二核苷酸与STING蛋白结合的主要因素。
本文要点
1)研究人员将结构生物学、等温量热法(ITC)和计算机模拟结合在一起,以阐明STING与六种环二核苷酸(CDN)结合的主要因素,这六种CDN其中包括三对天然(核糖)核苷酸和2'-氟代核糖的3,3'-CDN。
2){STING:CDN}配合物的X射线结构分析没有为所研究配体的亲和力不同提供任何解释。ITC显示,这组类似配体的熵/焓补偿高达25 kcal·mol-1。
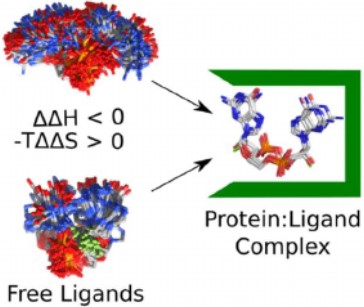
3)借助于计算机模拟,研究人员认为氟代核糖配体的较高亲和力可以通过结合时熵的损失较小以及张力(自由)能较小来解释。
参考文献:
Lubomí Miroslav Smola, et al. Ligand Strain and Its Conformational Complexity Is a Major Factor Determining Binding of Cyclic Dinucleotides to STING Protein. Angewandte Chemie, 2021.
DOI:10.1002/anie.202016805
https://onlinelibrary.wiley.com/doi/10.1002/anie.202016805


















