活性氧(ROS/RNS)在炎症过程中产生并引起蛋白修饰,但其免疫后果在很大程度上尚不清楚。在此,德国莱布尼茨低温等离子体研究所Sander Bekeschus等人利用能够产生不同种类的ROS/RNS的气体等离子体技术来模拟炎症,并利用模型蛋白鸡卵清蛋白(Ova vs oxOva)研究ROS/RNS修饰的意义。
本文要点:
1)动态光散射和圆二色谱揭示了oxOva与Ova相比的结构修饰。来自Ova特异性OT-II的T细胞,而不是来自C57BL/6或SKH-1野生型小鼠的T细胞在加入Ova后激活增强。oxOva在体外或体内给药时会加剧这种激活,同时增加干扰素-γ产生,这是一种已知的抗黑色素瘤药物。
2)对野生型小鼠进行oxOva疫苗接种,然后接种同源B16F10Ova表达的黑色素瘤细胞,结果表明,与用Ova疫苗接种的小鼠相比,T细胞的数量和激活增强,肿瘤负担减轻,抗原提呈细胞数量增加。
3)利用质谱分析oxOva识别出三个富含氧化修饰的热点区域,它们与增加的T细胞活化有关。
综上所述,利用Ova作为模型蛋白,多ROS/RNS修饰的免疫调节作用可能会刺激炎症研究和肿瘤疫苗策略的新研究路线。
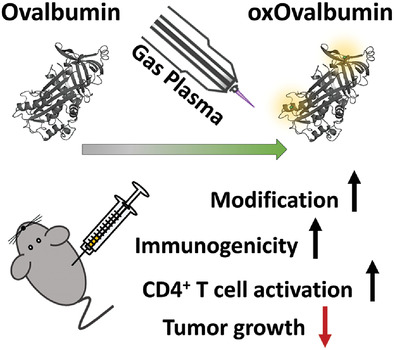
Ramona Clemen, et al. Gas Plasma Technology Augments Ovalbumin Immunogenicity and OT‐II T Cell Activation Conferring Tumor Protection in Mice. Adv. Sci., 2021.
DOI: 10.1002/advs.202003395
https://doi.org/10.1002/advs.202003395


















