细胞内翻译后修饰O-GlcNAc的一个主要作用是抑制蛋白质聚集。该领域以前的大多数研究都集中在淀粉样蛋白形成蛋白本身的O-GlcNAc修饰上。有鉴于此,美国南加利福尼亚大学的Matthew R. Pratt等研究人员,发现O-GlcNAc修饰小热休克蛋白可以增强其抗淀粉样蛋白伴侣活性。
本文要点
1)研究人员利用合成蛋白化学方法,发现O-GlcNAc还激活了某些小热休克蛋白(SHSP)的抗淀粉样蛋白活性,这是一种可能更重要的修饰事件,它可以广泛地发挥作用,并可在亚计量学上发挥作用。
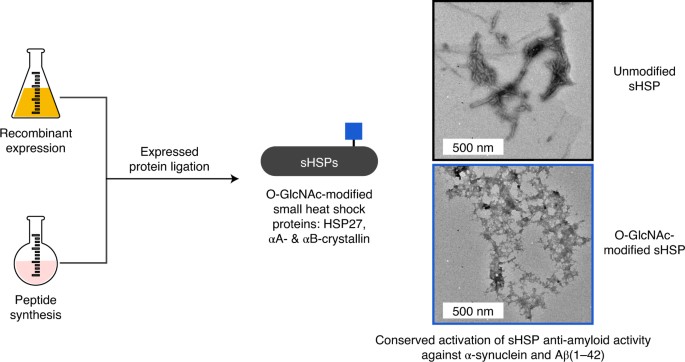
2)研究人员发现,O-GlcNAc能增强sHSPs对α-同核蛋白和Aβ(1-42)淀粉样蛋白形成的抑制能力。
3)从机理上讲,研究证明了在sHSP-IXI区附近的O-GlcNAc阻止了其分子内与底物结合的竞争能力。
4)研究发现,尽管阿尔茨海默病脑中的O-GlcNAc水平在总体上上降低了,但相关sHSP的修饰要么保持不变,要么增加,表明维持这些潜在保护性O-GlcNAc修饰的机制。
本文研究对淀粉样蛋白形成相关的神经退行性疾病以及sHSP生物学的其他领域都有重要的意义。
参考文献:
Aaron T. Balana, et al. O-GlcNAc modification of small heat shock proteins enhances their anti-amyloid chaperone activity. Nature Chemistry, 2021.
DOI:10.1038/s41557-021-00648-8
https://www.nature.com/articles/s41557-021-00648-8


















