通过外源性刺激诱导的代谢重编程灵活地控制癌细胞的命运,可以处理细胞可塑性衍生的治疗耐药性,这为在临床中治疗难治性和复发性肿瘤提供了有效的范例。在此,上海交通大学Wei Xue、Chunfu Zhang等人证明了适度的热量(45°C)可以显着降低抗氧化剂的表达,并触发与氧化铁纳米颗粒(Fe3O4 NPs)协同作用的癌细胞中特定脂质代谢的重新编程。
本文要点:
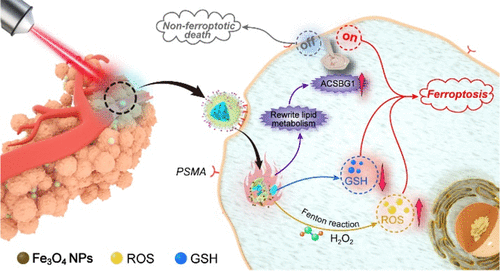
1)这种代谢控制行为破坏了肿瘤的氧化还原稳态,并产生了压倒性的脂质过氧化物,因此使肿瘤对铁死亡敏感。基于这些发现,通过合理设计多肽修饰的1H-全氟戊烷(1H-PFP)封装的含Fe3O4的纳米制剂(GBP@Fe3O4),提出了一种热触发的肿瘤特异的铁死亡治疗策略。
2)当用808 nm激光照射时,1H-PFP的相变由局部适度加热(45°C)触发,导致原位Fe3O4的突发释放,通过肿瘤微环境中的Fenton反应产生有效的活性氧。与抗氧化抑制反应和热应激引起的独特的脂质代谢重编程一起,这种氧化损伤被放大以诱导肿瘤铁死亡并获得足够的抗肿瘤作用。
3)重要的是,确认了酰基辅酶A合成酶ACSBG1是该热诱导的铁死亡过程中关键的促铁死亡因子。此外,该基因的敲除可以实现癌细胞死亡命运从铁死亡转变为非铁死亡死亡。
这项工作为原位热触发的铁死亡提供了机制和实用策略,以减少直接的铁死亡诱发剂的潜在副作用,并强调了在热应激下调节细胞命运的关键因素。
Shaowei Xie, et al. Metabolic Control by Heat Stress Determining Cell Fate to Ferroptosis for Effective Cancer Therapy, ACS Nano, 2021.
DOI: 10.1021/acsnano.1c00380
https://doi.org/10.1021/acsnano.1c00380


















