为了满足心脏再生医学的需求,需要在可扩展的悬浮培养系统中直接从人诱导多能干细胞(hiPSCs)中产生工程化的心脏组织。于此,美国奥本大学Elizabeth A. Lipke等人通过水凝胶封装的hiPSCs的直接分化成功生产功能性心脏组织微球。
本文要点:
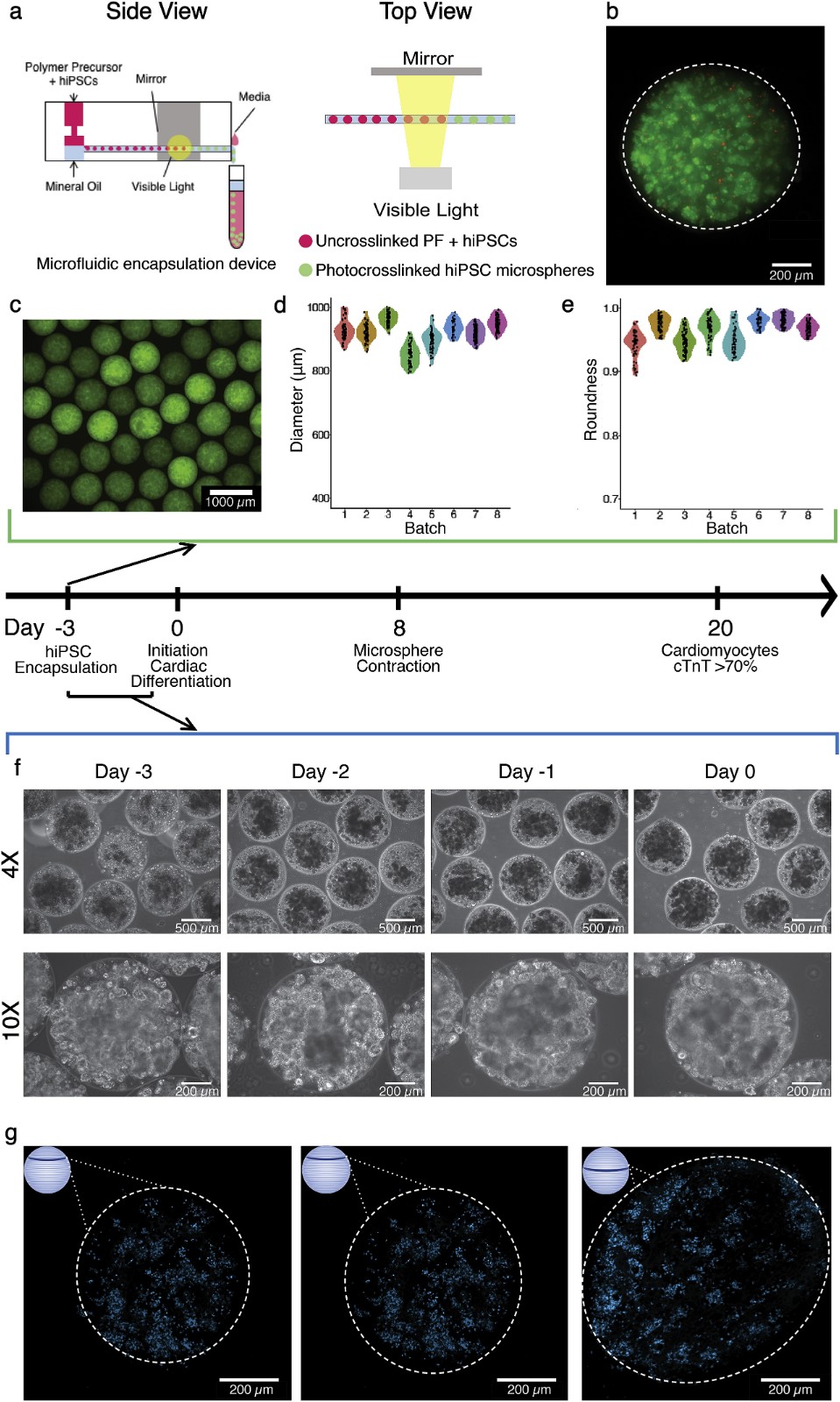
1)为了形成微球,将hiPSCs悬浮在光交联生物材料PEG纤维蛋白原(2500万细胞/mL)中,并使用定制的微流控系统以420000细胞/分钟的速率进行封装。即使在这样高的细胞密度和快速的生产速度下,也能获得高的批内和批间重现性。微球形成后,hiPSCs保持了较高的细胞活力,并在原PEG纤维蛋白原基质内外继续生长。这些最初柔软的微球(<250 pa)支持有效的心脏分化;在分化第8天开始自发收缩,并且微球含有>75%的心肌细胞(CMs)。
2)CMs对药理学刺激有适当的反应,当电起搏时,CMs表现出1:1的捕获率,高达6.0Hz。随着时间的推移,细胞形成细胞-细胞连接和排列的肌原纤维纤维;工程化的心脏微球在培养中维持了3年以上。快速生成均匀心肌微球组织的能力对于推进下游应用(包括生物制造、多孔板药物筛选和基于注射的再生疗法)至关重要。
参考文献:
Ferdous B. Finklea, et al., Engineered Cardiac Tissue Microsphere Production through Direct Differentiation of Hydrogel-encapsulated Human Pluripotent Stem Cells. Biomaterial 2021.
https://doi.org/10.1016/j.biomaterials.2021.120818


















