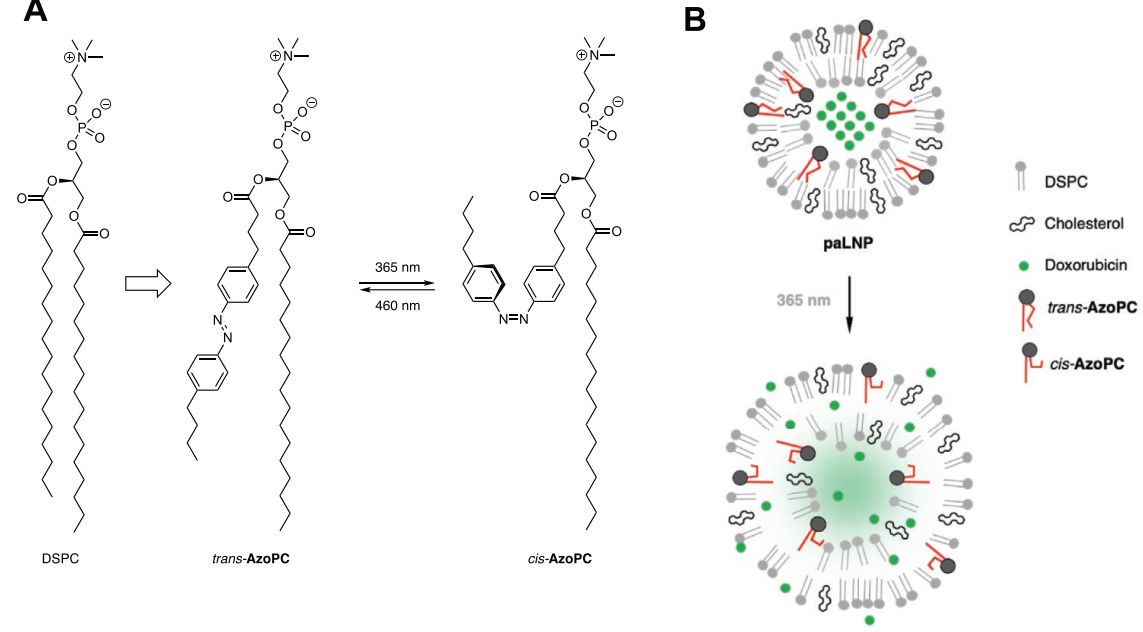
将小分子药物包埋在具有长循环时间的脂质纳米颗粒(LNPs)中可以减少其毒副作用并增强其在肿瘤部位的聚集。然而,这种策略也会使得药物很难从脂质体系统中被释放,从而导致治疗效果有限。因此,开发可在特定部位触发药物释放的方法是非常必要的。英属哥伦比亚大学Dominik Witzigmann、Pieter R. Cullis和纽约大学Dirk Trauner通过研究表明,在传统的LNPs中加入紫外线(UV-A)或红光可转换的磷脂酰胆碱类似物(AzoPC和redAzoPC)后所生成的光激活型LNPs(paLNPs)具有与父代DSPC-胆固醇脂质体相当的结构完整性、载药能力和尺寸大小。
本文要点:
(1)研究发现,该系统可在脉冲激光照射下通过偶氮苯的反式-顺式异构化以诱导释放65-70%的药物 (阿霉素)。体外实验结果表明,paLNPs在黑暗中是无毒的,但在光照射后会对人癌细胞产生细胞毒性。
(2)在斑马鱼胚胎中的体内研究表明,与临床批准的制剂相比,paLNPs具有显著延长血液循环时间,并能在脉冲光照射下增强药物释放。综上所述,paLNPs与临床批准的LNPs相比有着非常相似的特性,但它同时还具有光诱导药物释放的性能,这也使其具有很好的临床转化前景。
Nisha Chander. et al. Optimized Photoactivatable Lipid Nanoparticles Enable Red Light Triggered Drug Release. Small. 2021
DOI: 10.1002/smll.202008198
https://onlinelibrary.wiley.com/doi/10.1002/smll.202008198



















