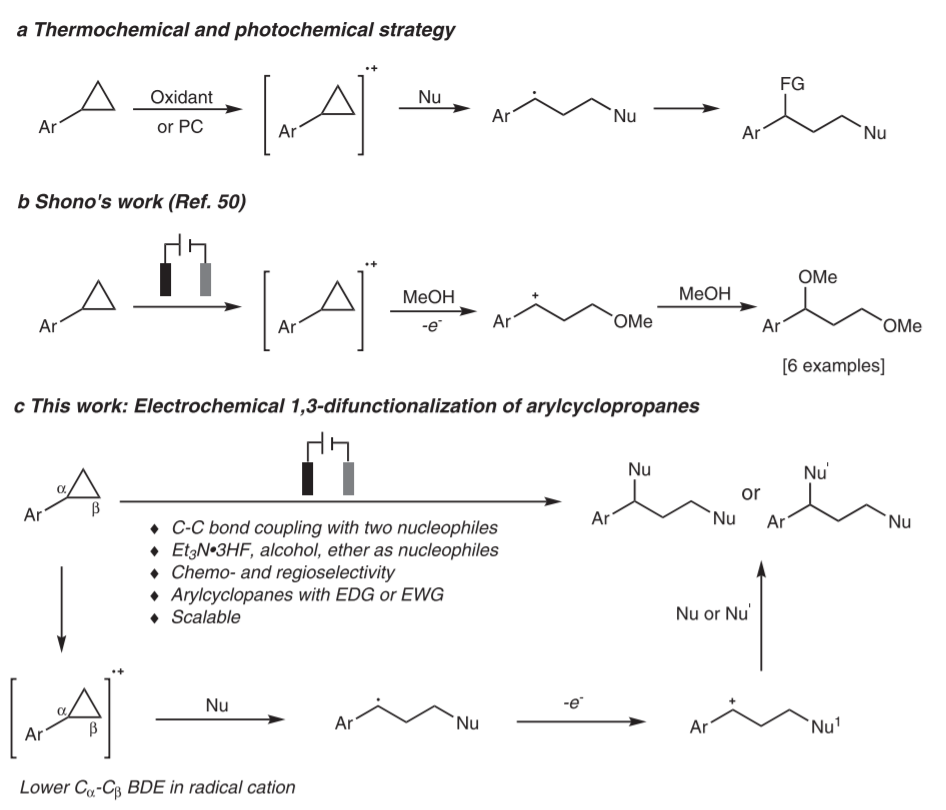
电化学在许多有机合成氧化还原反应中具有显著优势,但是在电化学C-C键切断、功能团化反应的方法学研究较为缺乏。有鉴于此,武汉大学雷爱文、张恒等报道发展一种电化学C-C切断、芳基环丙烷的1,3-双官能团化反应,该反应无需加入催化剂、氧化剂,通过选择合适的亲核试剂,通过该反应实现了1,3-双氟化、1,3-氟氧化、1,3-双氧化反应,该反应表现了优异的化学选择性和区域选择性,具有较好的官能团容忍性,能够实现规模化。反应机理研究结果显示,反应中在阳极上通过电化学氧化生成芳基环丙烷自由基阳离子,随后转化为苄基碳正离子中间体关键中间体,为构建1,3-双官能团化分子提供了一种简单有效的方法。
参考文献
Peng, P., Yan, X., Zhang, K. et al. Electrochemical C−C bond cleavage of cyclopropanes towards the synthesis of 1,3-difunctionalized molecules. Nat Commun 12, 3075 (2021).
DOI: 10.1038/s41467-021-23401-8
https://www.nature.com/articles/s41467-021-23401-8