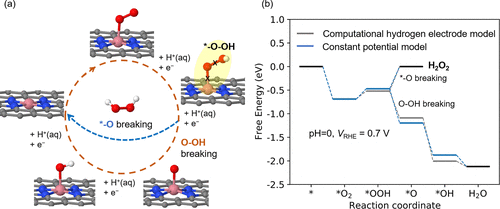
氧还原反应(ORR)是最重要的电化学反应之一。从常见的反应中间体*-O-OH 开始,ORR 分为两条途径,要么通过破坏 *-O 键产生过氧化氢 (H2O2),要么通过破坏 O-OH 键形成水。然而,令人费解的是,尽管许多催化剂对 O-OH 断裂具有强烈的热力学偏好,但为什么对过氧化氢表现出高选择性。此外,选择性取决于电势和 pH 值,这点仍未被理解。
有鉴于此,德克萨斯大学奥斯汀分校Yuanyue Liu等人,开发了一种先进的第一性原理模型,用于有效计算固体-水界面的电化学反应动力学,这是传统模型无法实现的。
本文要点
1)使用该模型研究用于生产 H2O2 的代表性催化剂,发现由于 O-OH 键的刚性,破坏 O-OH 键比破坏 *-O 键具有更高的能垒。重要的是,揭示了对电位和 pH 值的选择性依赖性植根于对 *-O-OH 中前/后 O 的质子亲和力。
2)对于单钴原子催化剂,降低电位会促进质子吸附到前一个 O 上,从而提高 H2O2 的选择性。相比之下,对于碳催化剂,质子更倾向于后者O,导致酸性条件下 H2O2 选择性较低。
3)这些发现解释了实验,并强调了选择性的动力学起源,揭示了质子亲和度作为一个新的因子,从而提高了对ORR的理解,并为有效模拟非均相电化学的原子级动力学提供了一个新的模型。
参考文献:
Xunhua Zhao et al. Origin of Selective Production of Hydrogen Peroxide by Electrochemical Oxygen Reduction. J. Am. Chem. Soc., 2021.
DOI: 10.1021/jacs.1c02186
https://doi.org/10.1021/jacs.1c02186


















