合成修饰蛋白质在药物和材料中的日益流行,暴露了对具有高位置选择性的化学修饰的有效策略的需求。虽然基因工程可以将非天然氨基酸引入重组蛋白中,但野生型蛋白的区域选择性化学修饰仍然是一个挑战。有鉴于此,美国普林斯顿大学的David W. C. MacMillan等研究人员,通过光氧化还原催化的位点选择性酪氨酸生物偶联用于天然到生物正交的蛋白质转化。
本文要点
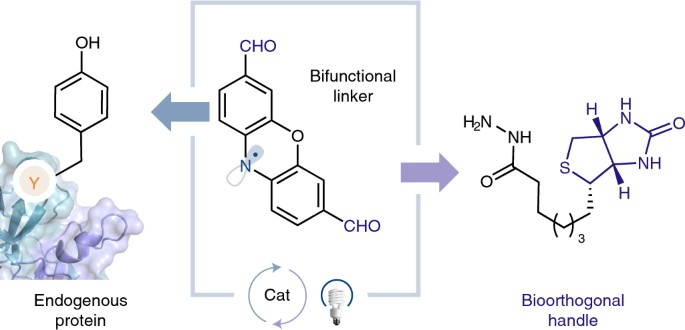
1)研究人员利用光氧化还原催化,开发了一种位点选择性酪氨酸生物偶联途径,该途径包含生物正交甲酰基团,随后允许从天然蛋白合成结构确定的荧光偶联物。
2)一种水溶性光催化剂,光黄素,已经被证明可以诱导先前未报道的吩恶嗪双醛标签和单一酪氨酸位点之间通过形成共价C-N键的氧化偶联,即使是在存在多个酪氨酸侧链的情况下。
3)研究人员证明多种天然蛋白质,包括那些含有多个酪氨酸的,可以成功地进行酪氨酸特异性和单位点选择性标记。
本文研究的技术直接将醛基引入天然蛋白,使产品快速多样化,形成一系列包括炔-叠氮化物点击反应的完善生物正交功能化方案。
参考文献:
Beryl X. Li, et al. Site-selective tyrosine bioconjugation via photoredox catalysis for native-to-bioorthogonal protein transformation. Nature Chemistry, 2021.
DOI:10.1038/s41557-021-00733-y
https://www.nature.com/articles/s41557-021-00733-y


















