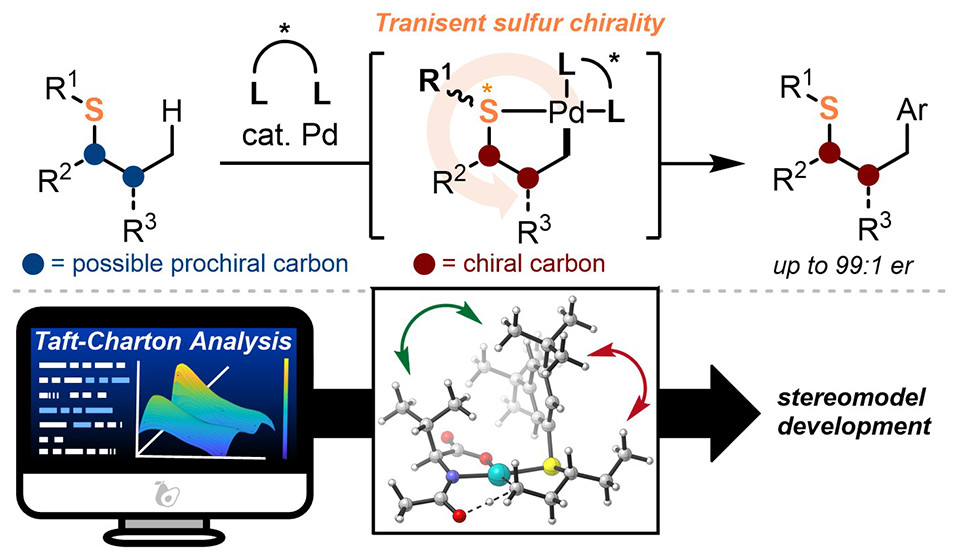
对映选择性C(sp3)-H键活化受到合成化学相关研究的广泛关注,虽然人们目前对此类C-H键活化反应产生非常大的兴趣,但是该反应中立体选择性机理并未得到很好的理解。作者在以往发展的硫醇导向C(sp3)-H键芳基化反应中发现配体和导向基团对反应非常敏感:当3-戊基硫化物作为前手性中心的α位点能够产生配体和导向基团有效进行,但是异丁基硫化物作为前手性中心的β位点没有反应。Scripps研究所余金权等报道,在定量化的结构-反应选择性分析中,作者通过导向基团、配体结构研究,发展了一系列N-乙酰基团保护氨基酸酰胺苯胺配体MPAAn,在硫醇导向C(sp3)-H芳基化反应中实现了较高的对映选择性(最高达到99:1)。
参考文献
Tyler G. Saint-Denis, Nelson Y. S. Lam, Nikita Chekshin, Paul F. Richardson, Jason S. Chen, Jeff Elleraas, Kevin D. Hesp, Daniel C. Schmitt, Yajing Lian, Chan Woo Huh, and Jin-Quan Yu*, Mechanistic Study of Enantioselective Pd-Catalyzed C(sp3)–H Activation of Thioethers Involving Two Distinct Stereomodels, ACS Catal. 2021, 11, 9738–9753
DOI: 10.1021/acscatal.1c02808
https://pubs.acs.org/doi/10.1021/acscatal.1c02808