澳大利亚昆士兰大学Carlos Salomon、Yusuke Yamauchi和Amirali Popat对用于新型药物递送的细胞外囊泡纳米结构相关研究进行了综述。
本文要点:
(1)细胞外囊泡(EVs)可以在各种病理或生理过程中传递细胞间信息,并将生物分子转运到受体细胞。与此同时,EVs也具有逃避免疫系统的能力,并能长期保持稳定,因此它们可以作为药物和生物制剂的天然载体。然而,EVs的分离、异质性、与同源生物分子共存以及缺乏位点特异性递送能力等挑战会阻碍其潜力的发挥。近年来,研究者提出将EVs与纳米结构相融合,并证明其可以实现有效的药物负载和位点特异性给药。随着纳米技术的发展,研究者开发出具有可调的大小、形状和表面性质的不同纳米结构与EVs相集成以用于药物负载、靶标结合、高效递送和治疗。这种整合能够提高对负载药物的保护和对细胞的靶向性,并将其特异性递送到靶细胞。
(2)作者在文中综述了近年来纳米结构与EVs的集成系统在给药、治疗和实时监测疾病进展方面的研究进展;随后,作者从外泌体载体、不同的药物递送系统和基于EVs的仿生纳米结构的选择性药物递送等方面对EVs仿生纳米结构的发展需求和面临的挑战进行了介绍,并对其未来前景进行了展望。
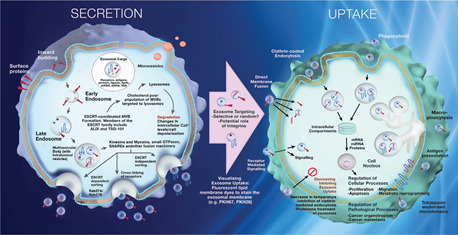
Shayna Sharma. et al. Extracellular Vesicle Nanoarchitectonics for Novel Drug Delivery Applications. Small. 2021
DOI: 10.1002/smll.202102220
https://onlinelibrary.wiley.com/doi/10.1002/smll.202102220



















