具有类酶特性的纳米材料的仿生设计已成为产生新型治疗药物的一种有希望的方法。然而,合成纳米材料同时保持对几何形状和价态的高度控制是一个突出的挑战。于此,南开大学黄兴禄等人介绍了一种基于纳米材料的合成生物学策略,该策略使用蛋白质构建块的“自下而上”分层结合,精确和定量地剪裁高有序纳米结构。
本文要点
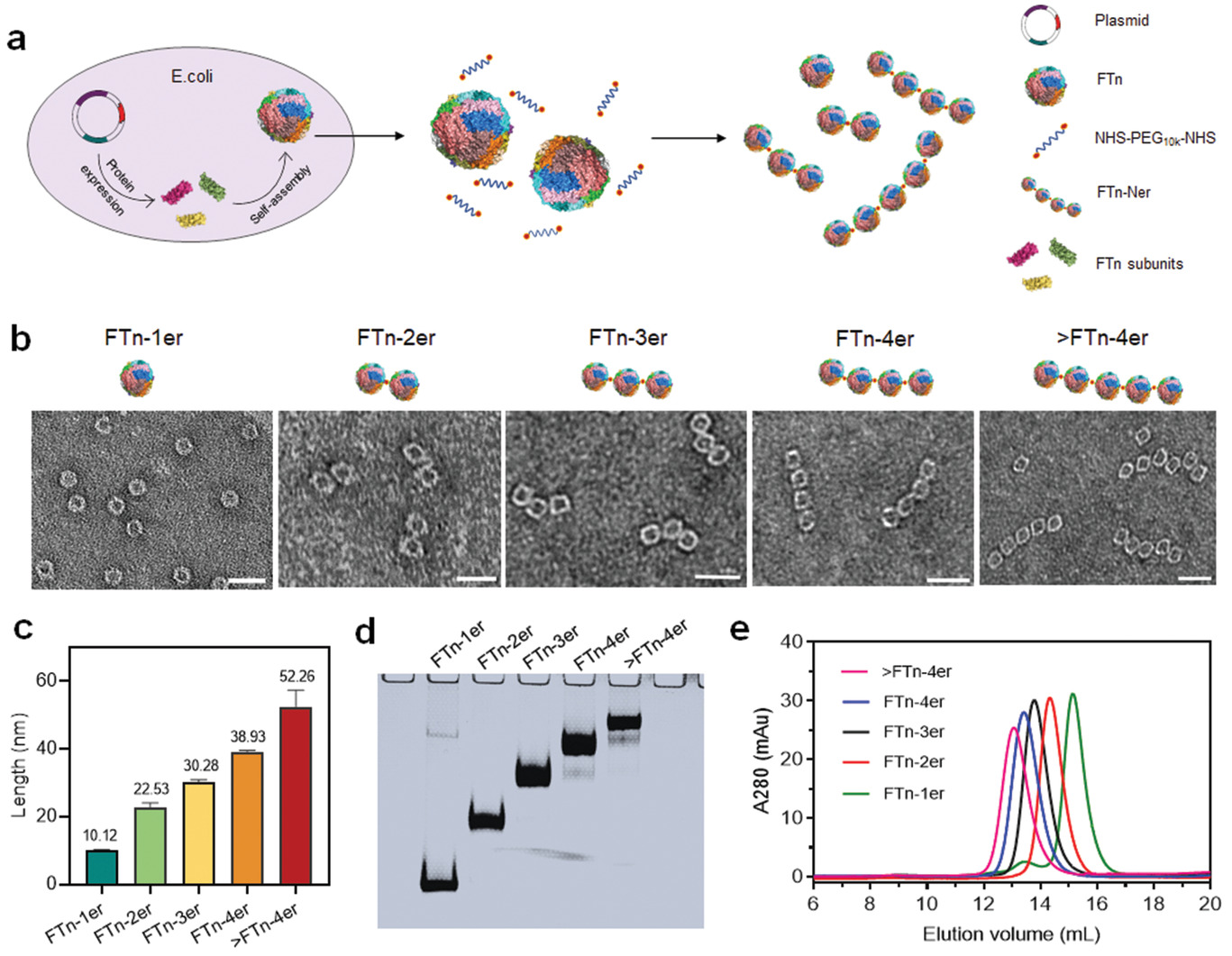
1)组装的纳米寡聚体具有可调节的蛋白质基序和多价结合域,有助于延长血液循环时间,通过直接靶向细胞受体在肿瘤细胞内积累,并通过转胞吞机制深入肿瘤组织。
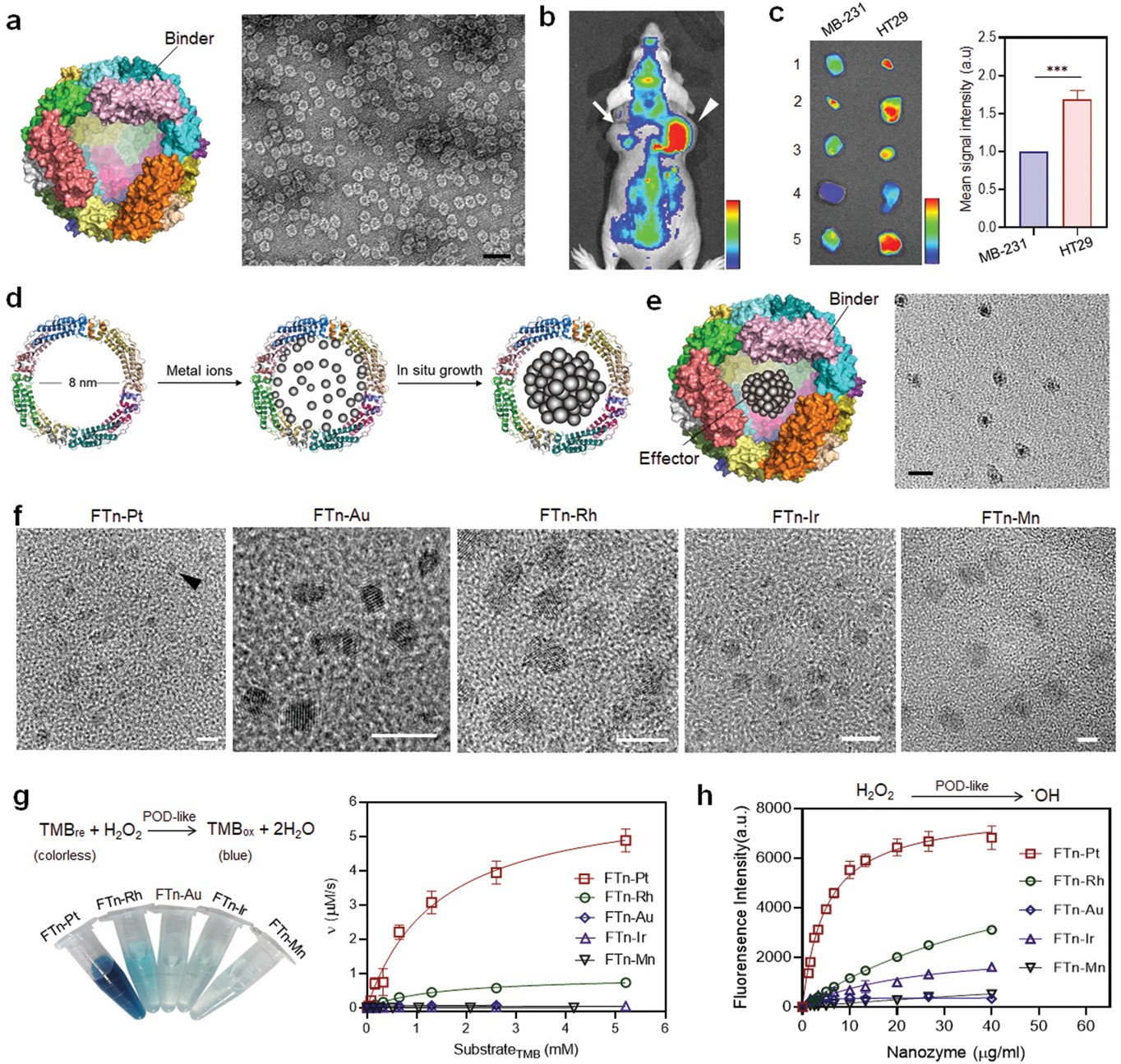
2)使用这些蛋白质/蛋白质纳米寡聚体作为支架,作者通过在蛋白质纳米笼的腔内原位掺入金属纳米簇,创造了一系列新的人工纳米级金属酶(纳米酶)。纳米酶能够模拟类似过氧化物酶活性并产生细胞毒性自由基。与单独的纳米酶相比,寡聚纳米酶的全身递送显示出显著增强的治疗和抗肿瘤益处。这项研究通过利用合成生物技术展示了对纳米技术的新见解。

参考文献:
Liu, Q., et al., Modular Assembly of Tumor-Penetrating and Oligomeric Nanozyme Based on Intrinsically Self-Assembling Protein Nanocages. Adv. Mater. 2021, 2103128.
https://doi.org/10.1002/adma.202103128


















