在一个40个残基的序列中,氨基酸的排列比地球上的原子还要多。该巨大的化学搜索空间阻碍了人类学习去设计功能性聚合物。有鉴于此,美国麻省理工学院的Bradley L. Pentelute等研究人员,报道了基于深度学习设计核靶向非生物微蛋白。
本文要点
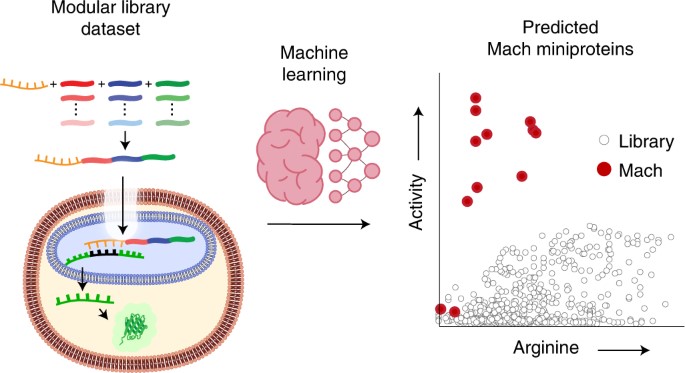
1)研究人员展示了机器学习如何使非生物核靶向微蛋白的从头设计能够将反义寡聚体输送到细胞核。
2)研究人员将高通量实验与定向进化启发的深度学习方法相结合,其中自然和非自然残基的分子结构表示为拓扑指纹图谱。
3)该模型能够预测训练数据集之外的活动,同时破译和可视化序列-活动预测。
4)被称为“Mach”的预测微蛋白的平均质量达到10kDa,比细胞中任何已知的变体都更有效,并且还可以将蛋白质输送到细胞质中。Mach微蛋白无毒,能在小鼠体内有效地传递反义物质。
本文研究结果表明,深度学习可以破译设计原理,产生高度活跃的生物分子,而这些分子不太可能被经验方法发现。
参考文献:
Carly K. Schissel, et al. Deep learning to design nuclear-targeting abiotic miniproteins. Nature Chemistry, 2021.
DOI:10.1038/s41557-021-00766-3
https://www.nature.com/articles/s41557-021-00766-3


















