无机纳米医学以其优异的生物相容性和可调、多用途的功能而日益受到生物医学领域研究者的关注。然而,这些纳米药物在靶向组织中相对较差的积累和保留往往会严重阻碍它们的临床转化。澳门大学王瑞兵教授以葫芦[7]脲包被的Fe3O4 NPs为人工靶点,通过磁性作用将其沉积到肿瘤中,进而实现了二茂铁(Fc)包被的Au NPs在肿瘤中的高效靶向递送和原位聚集。
本文要点:
(1)研究表明,CB[7]-Fc主客体相互作用(研究者首次将其定义为超分子趋向性)能够使得这些Au NPs在肿瘤中实现大量的积聚和保留。
(2)体内外研究表明。Au NPs可在肿瘤细胞和组织中通过超分子趋向性和原位聚集实现精确可控的特异性积累和保留,进而能够对癌症进行局部增强CT成像和肿瘤特异性光热治疗。综上所述,这一研究这提出了一个超分子趋向性的新概念,它可用于驱动靶向递送和实现纳米药物的特异性积累、保留和激活,进而有效地改善生物成像和癌症治疗。
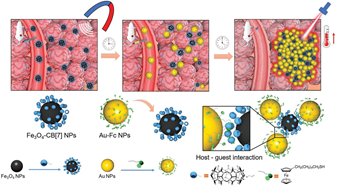
Qian Cheng. et al. Supramolecular Tropism Driven Aggregation of Nanoparticles In Situ for Tumor-Specific Bioimaging and Photothermal Therapy. Small. 2021
DOI: 10.1002/smll.202101332
https://onlinelibrary.wiley.com/doi/10.1002/smll.202101332



















