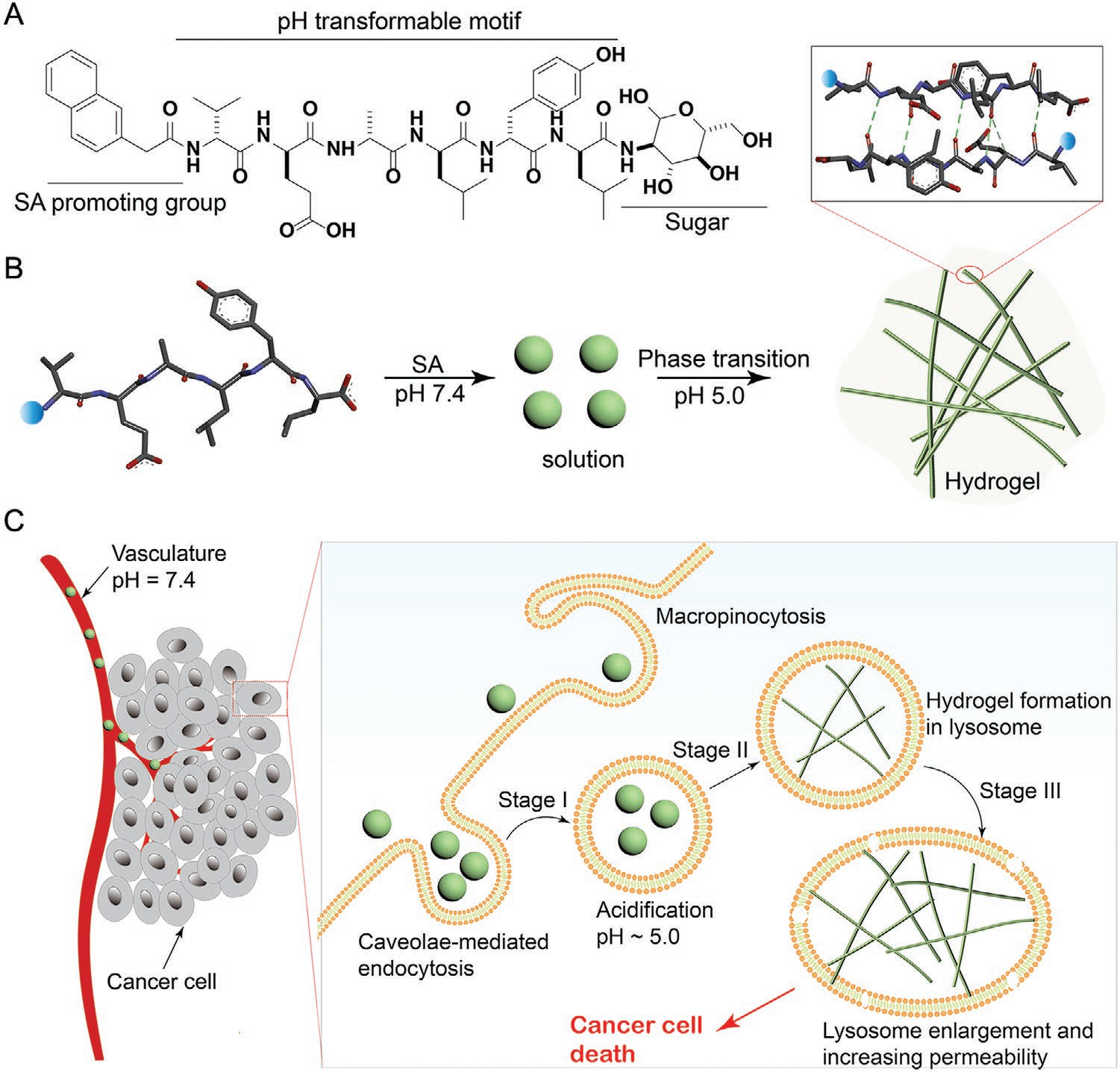
生物分子凝聚体是生物系统中所普遍存在的现象,其在控制细胞功能方面也发挥着重要作用。然而,如何实现功能性人工生物分子凝聚体的时空构建仍然具有挑战性,且相关的研究探索也较少。西湖大学王怀民研究员报道了一种在活细胞溶酶体中构建生物分子凝聚体(如水凝胶)以用于癌症治疗的一般方法,并基于此解决了由溶酶体隔离所引起的癌症多重耐药性。
本文要点:
(1)实验所构建的pH响应型六肽(LTP)可主要通过依赖于小泡的内吞作用而被癌细胞摄取,进而使得LTP会在溶酶体内发生由质子触发的相转化(溶液到水凝胶)。研究表明,在溶酶体内形成的水凝胶会进一步导致癌细胞中溶酶体的增大,并且增加溶酶体的渗透性,以导致癌细胞死亡。
(2)实验结果表明,该溶酶体组装可以显著提高现有化疗药物在体外和异种移植瘤模型中对抗耐多药(MDR)肿瘤细胞的效率。综上所述,这一工作为精确控制活细胞细胞器中功能性凝聚体的形成和解决癌症治疗所面临的MDR问题提供了一种新的解决策略。
Jing Wang. et al. Intracellular Condensates of Oligopeptide for Targeting Lysosome and Addressing Multiple Drug Resistance of Cancer. Advanced Materials. 2021
DOI: 10.1002/adma.202104704
https://onlinelibrary.wiley.com/doi/10.1002/adma.202104704



















