1 型脊髓小脑共济失调的RNAi可以预防和逆转小鼠模型中的行为缺陷和神经病理学读数、安全性和益处持续数月。由AAV.miS1表达的 RNAi 触发器也纠正了错误调节的 miRNA,例如 miR150。有鉴于此,美国费城研究所儿童医院的Beverly L. Davidson等研究人员,报道了AAV 将RNA 干扰 (RNAi)表达构建体递送到非人灵长类动物大脑后的毒性。
本文要点
1)研究人员证明了递送方法是可扩展的,并且腺相关病毒载体 (AAV.miS1)在短期非人类灵长类动物 (NHP) 试点研究中是安全的。
2)为了将这项技术推向患者,在 NHP 中启动了研究性新药 (IND) 研究。
3)在将 AAV.miS1 递送到小脑深部细胞核后,意外地观察到了小脑毒性。
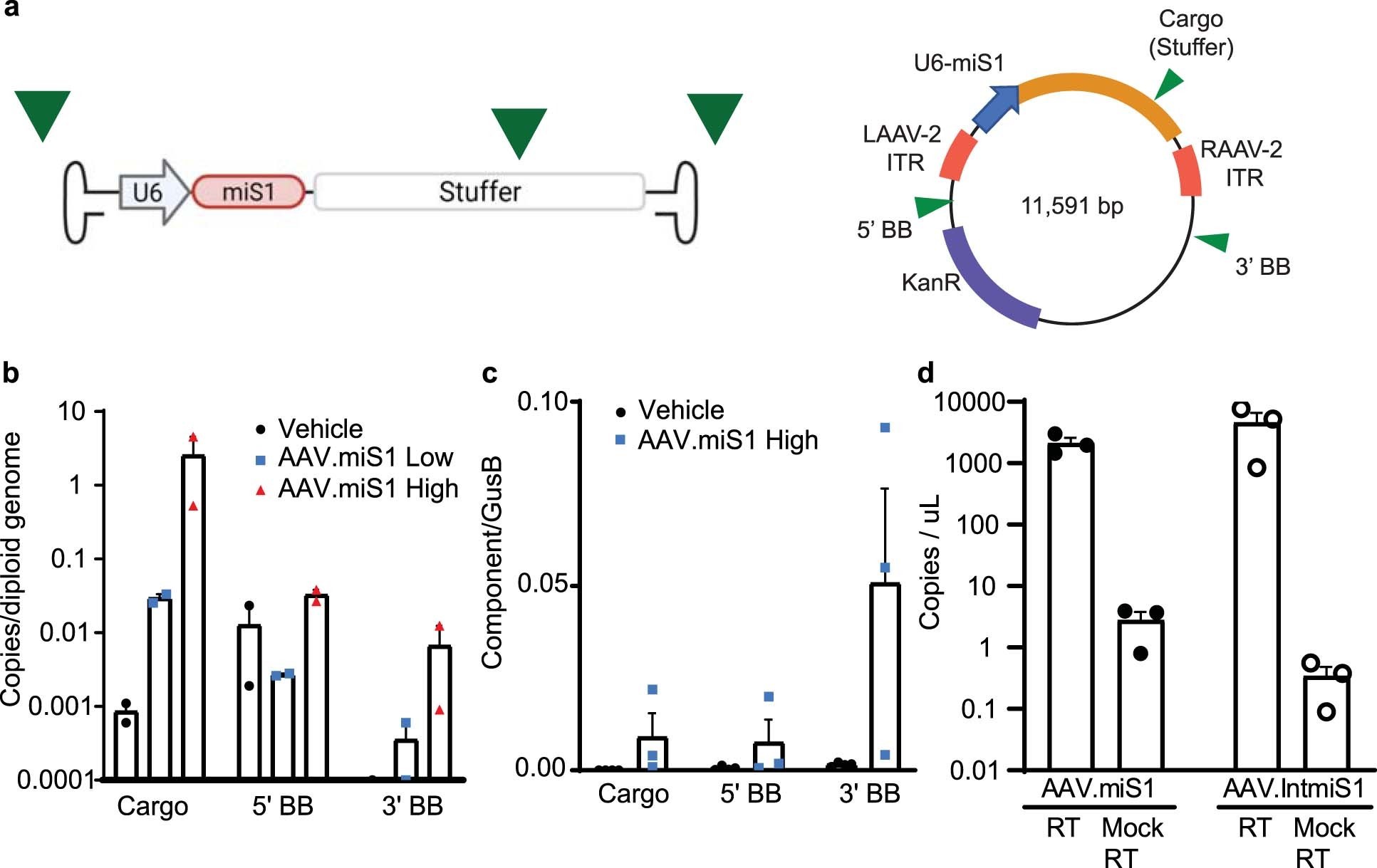
4)小RNA-seq 和使用不含microRNA (miRNA)的 AAV 的研究都表明,这不是内源性 miRNA 加工机制饱和的结果。
5)RNA-seq 连同 AAV 产品的测序表明,尽管交叉包装的材料数量有限,但仍有大量与神经病理学相关的反向末端重复 (ITR) 启动子活性。通过改变 miS1 表达环境降低了 ITR 启动子活性。
本文研究的啮齿动物和 NHP 研究结果之间令人惊讶的对比突出了在评估用于人类应用的新疗法时对多个物种进行扩展安全性研究的必要性。
参考文献:
Megan S. Keiser, et al. Toxicity after AAV delivery of RNAi expression constructs into nonhuman primate brain. Nature Medicine, 2021.
DOI:10.1038/s41591-021-01522-3
https://www.nature.com/articles/s41591-021-01522-3


















