来自共生微生物群的小分子对肠道免疫的成熟和调节起着至关重要的作用。然而,对于在宿主-微生物群环境中控制免疫发展的分子机制知之甚少。有鉴于此,美国哈佛医学院的Dennis L. Kasper、Sungwhan F. Oh、韩国首尔大学的Seung Bum Park等研究人员,发现肠道共生菌群能够通过膳食氨基酸产生调节宿主免疫的脂质。
本文要点
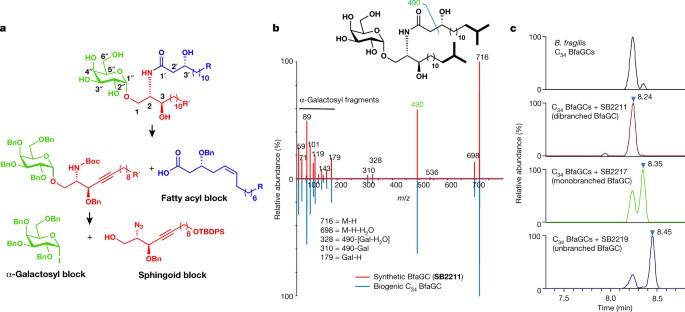
1)研究人员使用靶向脂质组分析和合成方法,对来自人类共生体脆弱拟杆菌(Bacteroides fragilis)的免疫调节性α-半乳糖基神经酰胺(BfaGCs)进行了多方面的调查。
2)BfaGCs的特征性末端支链是脆弱拟杆菌在宿主肠道中吸收支链氨基酸的结果。
3)一个不能代谢支链氨基酸的脆弱拟杆菌基因敲除株显示BfaGCs的支链减少,并且只定植这种突变株的小鼠的自然杀伤T(NKT)细胞调节功能受损,这意味着结构特异的免疫调节活性。
4)BfaGCs的鞘氨醇链支链是NKT细胞激活的一个关键决定因素,它能诱导特定的免疫调节基因表达特征和效应功能。
5)CD1d-BfaGC-NKT细胞受体复合物的共结晶结构和亲和力分析证实了BfaGCs作为CD1d限制性配体的互动。
本文研究提出了一个通过内生代谢物与饮食、微生物群和免疫系统的相互作用实现免疫调节控制的新范式。
参考文献:
Sungwhan F. Oh, et al. Host immunomodulatory lipids created by symbionts from dietary amino acids. Nature, 2021.
DOI:10.1038/s41586-021-04083-0
https://www.nature.com/articles/s41586-021-04083-0


















