胞苷脱氨酶 (AID)催化免疫球蛋白基因内的脱氧胞苷脱氨为脱氧尿嘧啶,从而诱导体细胞超突变和类别转换重组。AID 产生的脱氧尿嘧啶被颠覆的碱基切除和错配修复途径识别和加工,确保在 B 细胞中产生诱变结果。然而,为什么这些 DNA 修复途径不能准确修复 AID 诱导的病变仍然未知。有鉴于此,加拿大多伦多大学的Alberto Martin等研究人员,揭示FAM72A 拮抗尿嘧啶 DNA 糖基化酶 2 (UNG2) 以促进抗体成熟过程中的诱变修复。
本文要点
1)研究人员使用全基因组 CRISPR 筛选显示 FAM72A 是脱氧尿嘧啶易错加工的主要决定因素。
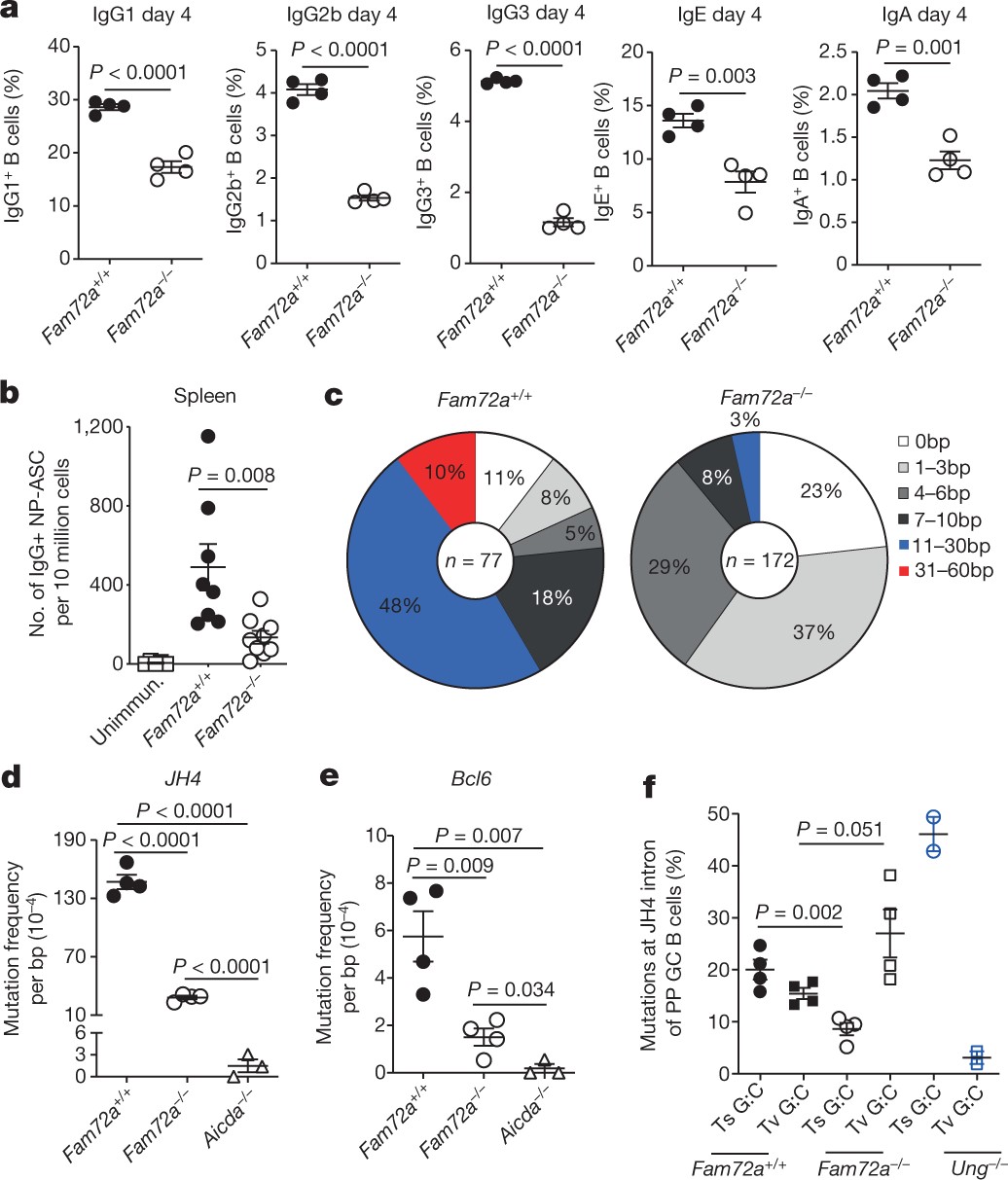
2)来自 Fam72a-/- 小鼠的 Fam72a 缺陷型 CH12F3-2 B 细胞和原代 B 细胞表现出免疫球蛋白和 Bcl6 基因的类别转换重组和体细胞超突变频率降低,以及全基因组脱氧尿嘧啶降低。
3)Fam72a-/- 小鼠 B 细胞中的体细胞超突变谱与在UNG2缺陷小鼠中观察到的相反,这表明 UNG2 在 FAM72A 缺陷细胞中过度活跃。
4)FAM72A 与 UNG2 结合,导致细胞周期 G1 期 UNG2 蛋白水平降低,与激活诱导的胞苷脱氨酶 (AID)活性峰值一致。
5)FAM72A 会导致 U·G 错配持续进入 S 阶段,导致通过错配修复进行易错修复加工。通过禁用通常从 DNA 中有效去除脱氧尿嘧啶的 DNA 修复途径,FAM72A 使 AID 能够充分发挥其对抗体成熟的影响。
本文研究工作对肿瘤有影响,因为在许多肿瘤中观察到的 FAM72A 过表达可以促进诱变。
参考文献:
Yuqing Feng,et al. FAM72A antagonizes UNG2 to promote mutagenic repair during antibody maturation. Nature, 2021.
DOI:10.1038/s41586-021-04144-4
https://www.nature.com/articles/s41586-021-04144-4


















