聚合物代表了肝外信使 RNA (mRNA) 递送的有前景的治疗平台,但由于复合物血清不稳定性和全身给药后内体逃逸不足而受到体内疗效低下的阻碍。
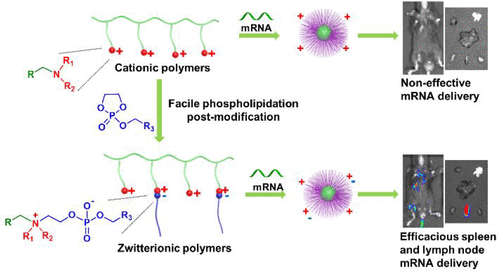
鉴于此,德克萨斯大学西南医学中心Daniel J. Siegwart等人报道了通过烷基化二氧磷杂环戊烷氧化物对阳离子聚合物进行后修饰以在体内将mRNA传递到脾脏和淋巴结的两性离子磷脂聚合物(ZPP)的合理设计和组合合成。成果发表在JACS上。
本文要点:
1)这种模块化的后修饰方法很容易产生用于血清抗性的可调两性离子物种,并同时引入烷基链以增强内体逃逸,从而将有缺陷的阳离子聚合物转化为有效的两性离子 mRNA 载体,而无需精心合成功能单体。
2)ZPPs 在体外介导的蛋白质表达比其亲本阳离子对应物高出39500 倍,并且在体内静脉内给药后能够在脾脏和淋巴结中选择性地有效传递 mRNA。这种两性离子磷脂化方法提供了一种通用且可推广的后修饰策略,将两性离子引入阳离子聚合物的侧链,扩展了阳离子聚合物家族在精确 mRNA 递送方面的实用性,并展示了免疫治疗应用的巨大潜力。
参考文献:
Zwitterionic Phospholipidation of Cationic Polymers Facilitates Systemic mRNA Delivery to Spleen and Lymph Nodes. JACS 2021.
https://pubs.acs.org/doi/abs/10.1021/jacs.1c09822


















