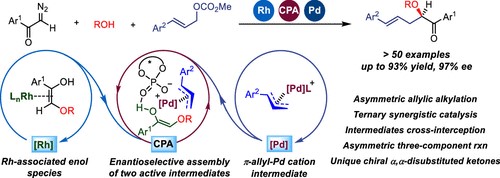
在合成化学中,通过Aldol、Mannich和Michael加成与相应的台架稳定受体阻断叶立德铵的多组分反应得到了广泛的应用。然而,由于这些原位生成的中间体具有较高的反应活性和瞬时存活率,取代型截获过程,尤其是不对称催化型截获过程,至今仍然未知。有鉴于此,中山大学的胡文浩、Xinfang Xu和南京大学的Yong Liang等研究人员,报道了三元催化使三组分不对称烯丙基烷基化成为手性α,α-双取代酮的简明途径。
本文要点
1)研究人员通过采用非手性钯络合物Rh2(OAc)4和手性磷酸CPA的三元协同催化,报告了α-重氮羰基化合物与醇和碳酸烯丙酯的三组分不对称烯丙基化反应。
2)该方法代表了通过SN1型捕获过程进行的三组分不对称烯丙基烷基化的首个示例,该过程涉及两种活性中间体的聚合组装,Pd烯丙基物种和源自叶立德铵的烯醇,提供了快速获得手性α,α-二取代酮的方法,具有较高的产率和极好的对映选择性。
3)综合实验和计算研究揭示了该新型三组分反应的机理,包括Xantphos配体的关键作用和对映选择性的起源。
参考文献:
Zhenghui Kang, et al. Ternary Catalysis Enabled Three-Component Asymmetric Allylic Alkylation as a Concise Track to Chiral α,α-Disubstituted Ketones. JACS, 2021.
DOI:10.1021/jacs.1c09148
https://pubs.acs.org/doi/10.1021/jacs.1c09148


















