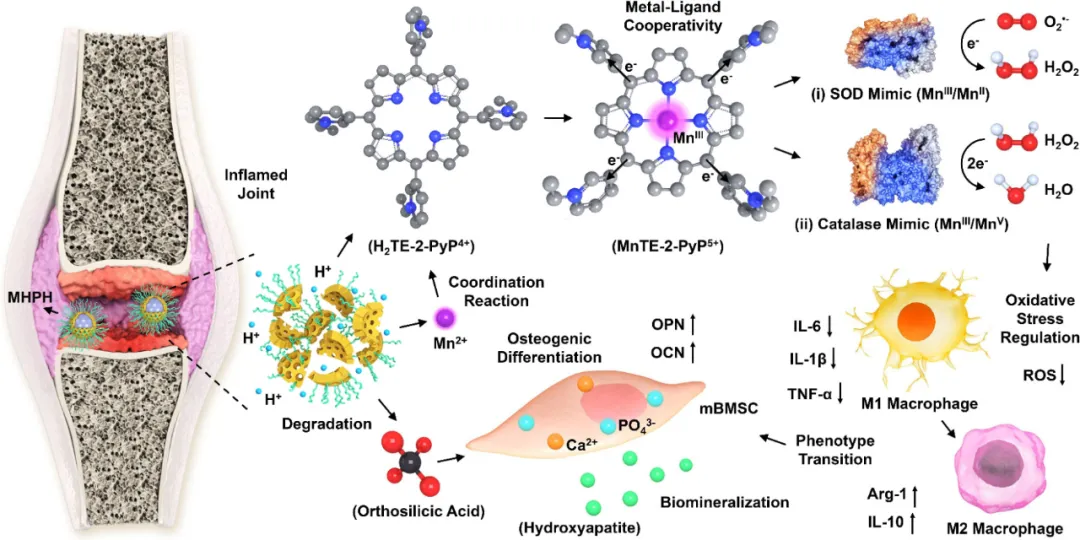
模拟天然酶的活性金属位点的配位几何结构是设计具有类酶体内反应热力学和动力学的治疗化学品的有效策略。鉴于此,以类风湿性关节炎(一种常见且难以治愈的免疫介导疾病)为例,中科院上海硅酸盐研究所施剑林院士等人将这种化学概念应用于天然抗氧化酶模拟物的原位合成,用于催化抗炎治疗。成果发表在JACS上。
简而言之,首先通过将阳离子卟啉配体装载到锰工程化介孔二氧化硅纳米载体中构建复合纳米药物,该载体可以响应弱酸性环境同时释放锰离子和卟啉配体,使其随后能够与活性锰位点的配位环境(类似于天然超氧化物歧化酶(SOD)和过氧化氢酶中的金属位点)进行配位和合成锰卟啉。
由于在 N4-大杂环的中间位置四取代的N-乙基吡啶鎓-2-基基团实现了强金属-配体交换偶联,这种锰卟啉通过通过外球面-质子耦合单电子转移(diaquamanganese(III)/monoaquamanganese(II)循环)表现出歧化超氧阴离子的SOD样活性,以及通过内球质子耦合双电子转移(diaquamanganese(III)/dioxomanganese(V) 循环)表现出歧化过氧化氢的过氧化氢酶样活性。
细胞实验证明了复合纳米药物通过促进 M1 巨噬细胞向抗炎 M2 表型的极化转变而具有高抗氧化功效。同样重要的是,从硅酸锰纳米载体释放的含硅低聚物可以作为羟基磷灰石的异质成核中心,促进骨间充质干细胞的生物矿化。最后,体内佐剂诱发的关节炎动物模型进一步揭示了纳米药物治疗类风湿性关节炎的高效性。
参考文献:
In Situ Synthesis of Natural Antioxidase Mimics for Catalytic Anti-Inflammatory Treatments: Rheumatoid Arthritis as an Example. J. Am. Chem. Soc. 2021.
https://doi.org/10.1021/jacs.1c09993


















