纳米材料能够在单一的纳米平台上结合多模态成像和治疗功能,因此在分子药物和生物应用方面引起了研究者的广泛关注。北京大学戴志飞教授构建了一个基于尺寸相对较小(<20nm)、负载卟啉接枝脂质的氧化铁纳米粒子的诊疗平台(Fe3O4@PGL NPs)。
本文要点:
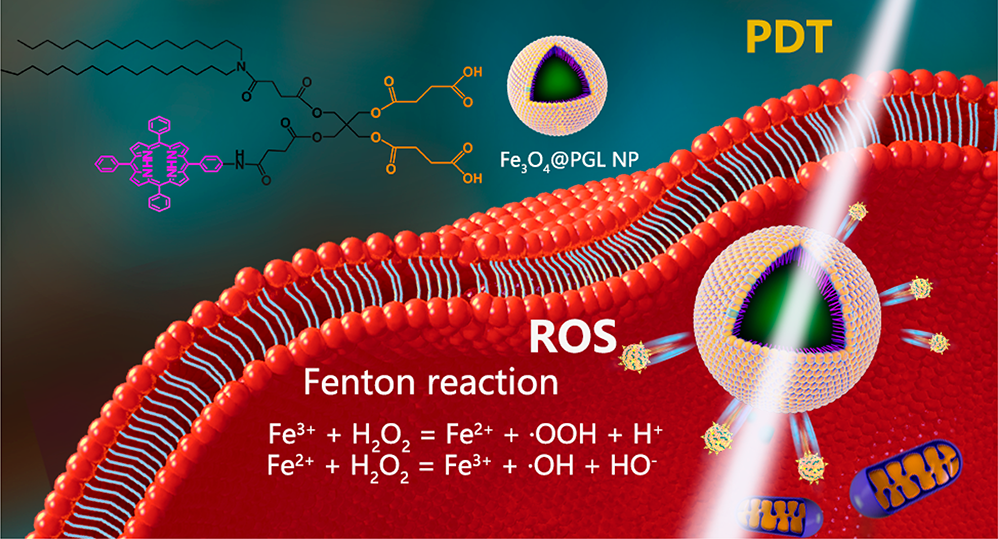
(1)两亲性PGL能够在超小尺寸的Fe3O4 NPs的疏水外表面进行自组装,最终得到直径为10 nm的Fe3O4@PGL NPs。实验所合成的PGL NPs具有优异的自组装特性,能够有效负载卟啉,且暗毒性极低,能够在体外对HT-29癌细胞表现出优异的光动力效应。体内实验结果表明,Fe3O4@PGL NPs可通过荧光和磁共振(MR)成像以示踪NPs的生物分布和治疗反应,并能同时触发产生高细胞毒性的活性氧(ROS)以实现光动力治疗(PDT)。
(2)随后,实验进一步评估了Fe3O4@PGL NPs/Fe3O4@Lipid NPs通过调节肿瘤微环境(TME)以实现铁死亡治疗(FT)和增强抗癌活性的能力。研究人员推测,肿瘤相关巨噬细胞(TAMs)可以通过在体外加速类芬顿反应而显著提高FT的疗效。实验结果表明,体外释放的Fe离子可以直接促进类芬顿反应,而荧光成像结果则说明RAW 264.7巨噬细胞的存在会进一步加速ROS的生成。被HT-29细胞和RAW264.7细胞所内吞的NPs会在共孵育过程中诱导ROS的显著增加,进而对癌细胞产生增强的细胞毒性。
Xiaolong Liang. et al. Complementing Cancer Photodynamic Therapy with Ferroptosis through Iron Oxide Loaded Porphyrin-Grafted Lipid Nanoparticles. ACS Nano. 2021
DOI: 10.1021/acsnano.1c08108
https://pubs.acs.org/doi/10.1021/acsnano.1c08108



















