基于不同细胞死亡机制的联合治疗能够有效提高对肿瘤的治疗效果。然而,目前研究者在设计时相关药物时往往对于不同的治疗模式的整合缺乏合理的理论依据,因此难以最大程度地发挥协同治疗的效果。厦门大学周子健副教授、浙江大学附属第四医院唐龙光研究员和新加坡国立大学陈小元教授通过仔细探究铁死亡和光热治疗的联合作用机制,设计了一种新型纳米诊疗药物。
本文要点:
(1)实验将克酮酸菁分子作为光热转换试剂和铁螯合剂,利用牛血清白蛋白对其进行包裹,从而构建了具有良好生物相容性的Cro-Fe@BSA纳米粒子。Cro-Fe@BSA纳米颗粒在肿瘤环境中具有可激活的光热效应。由于类芬顿反应具有温度依赖性,因此光热效应能够促进自由基的形成;而铁死亡过程中产生自由基则能够破坏热诱导形成的热休克蛋白,从而解决癌细胞对于热的自我保护机制。
(2)研究表明,这种“互惠互利”的策略能够在体外和皮下小鼠肿瘤模型中实现高效的抗癌作用。此外,Cro-Fe@BSA纳米粒子也能够实现可激活的光声和磁共振成像。综上所述,这项研究能够为协同不同的治疗方式以设计新型高效的纳米诊疗药物提供新的策略。
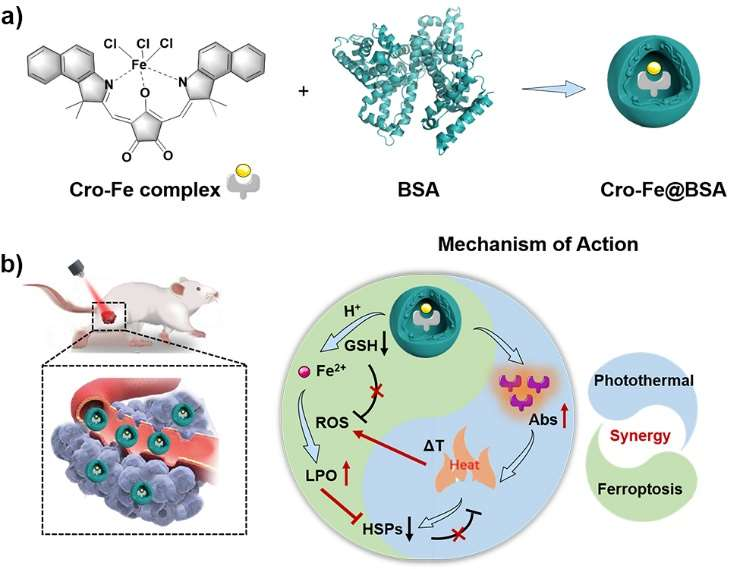
Fantian Zeng. et al. Coordinating the Mechanisms of Action of Ferroptosis and Photothermal Effect for Cancer Theranostics. Angewandte Chemie International Edition. 2021
DOI: 10.1002/anie.202112925
https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.202112925



















