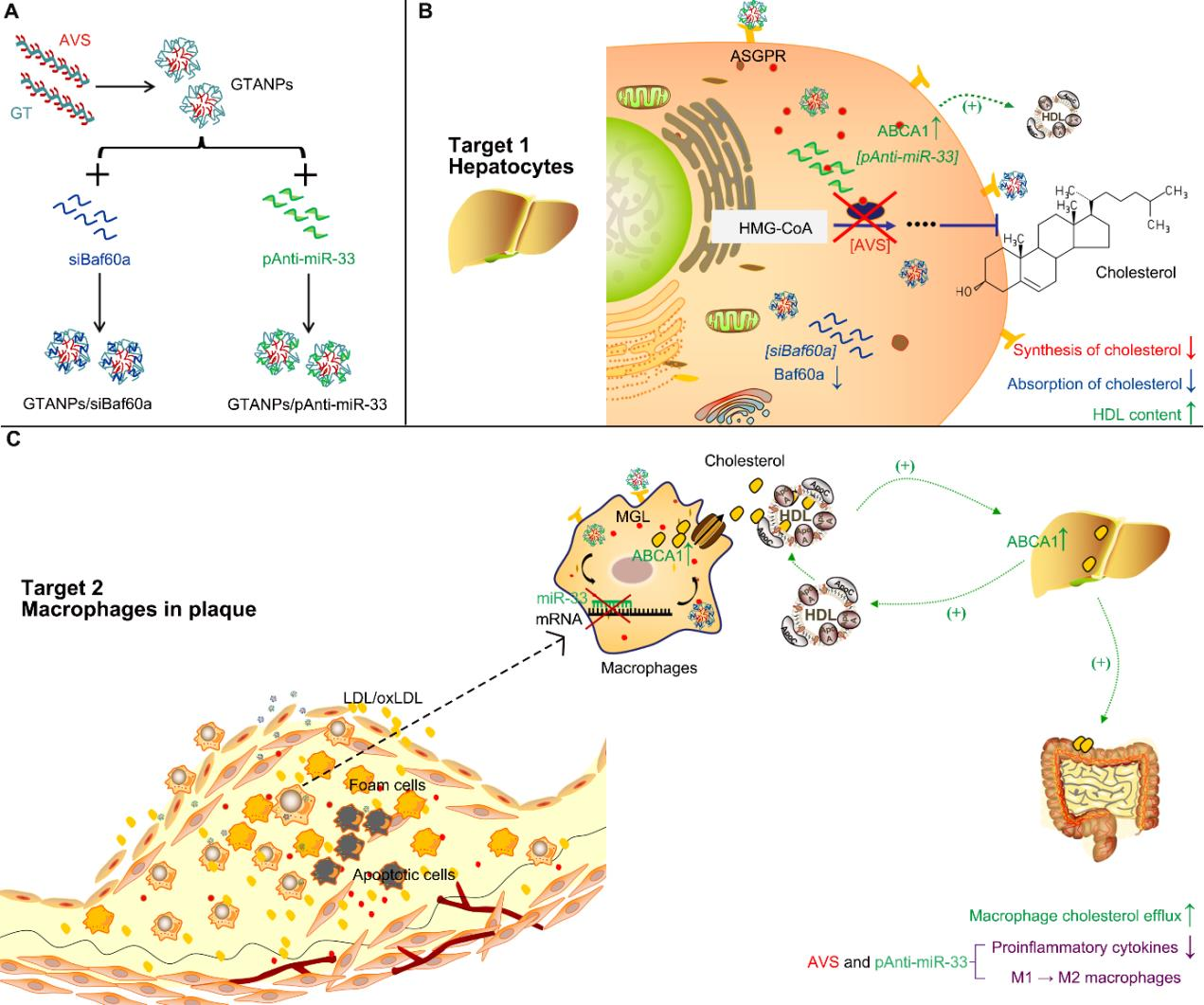
动脉粥样硬化引起的心血管疾病具有很高的发病率和死亡率。由于同时递送他汀类药物与核酸能够协同调节胆固醇代谢和病变炎症,因此该策略可以有效缓解动脉粥样硬化。有鉴于此,复旦大学印春华教授制备了能够双靶向肝细胞和损伤巨噬细胞的阿托伐他汀和半乳糖修饰的三甲基壳聚糖纳米颗粒(GTANPs),并将其用于封装Baf60a siRNA(siBaf60a)和anti-miR-33 pDNA(pAnti-miR-33),以实现对他汀类药物和核酸的有效共递送。
本文要点:
(1)研究表明,GTANPs/siBaf60a和GTANPs/pAnti-miR-33具有体外抗炎和脂质调节作用。在敲除ApoE的动脉粥样硬化小鼠中,静脉注射GTANPs/siBaf60a能够协同降低血浆胆固醇和动脉粥样硬化的斑块面积。
(2)与此同时,口服GTANPs/pAnti-miR-33则能够协同提高血浆高密度脂蛋白胆固醇(HDL-C)和抗炎细胞因子的水平,从而实现良好的抗动脉粥样硬化效果。综上所述,这一研究为实现他汀类药物和核酸的协同递送以治疗动脉粥样硬化提供了一个新的策略。
Ting Jiang. et al. Dual targeted delivery of statins and nucleic acids by chitosan-based nanoparticles for enhanced antiatherosclerotic efficacy. Biomaterials. 2021
https://www.sciencedirect.com/science/article/pii/S0142961221006803



















