尽管tRNA生物生成的失调促进了癌症中促肿瘤发生的mRNA的翻译,但对肿瘤发生中tRNA失调的机制和后果还不甚了解。有鉴于此,美国纽约大学的Iannis Aifantis、Palaniraja Thandapani等研究人员,发现缬氨酸tRNA水平和可用性调节白血病中复合物I的组装。
本文要点
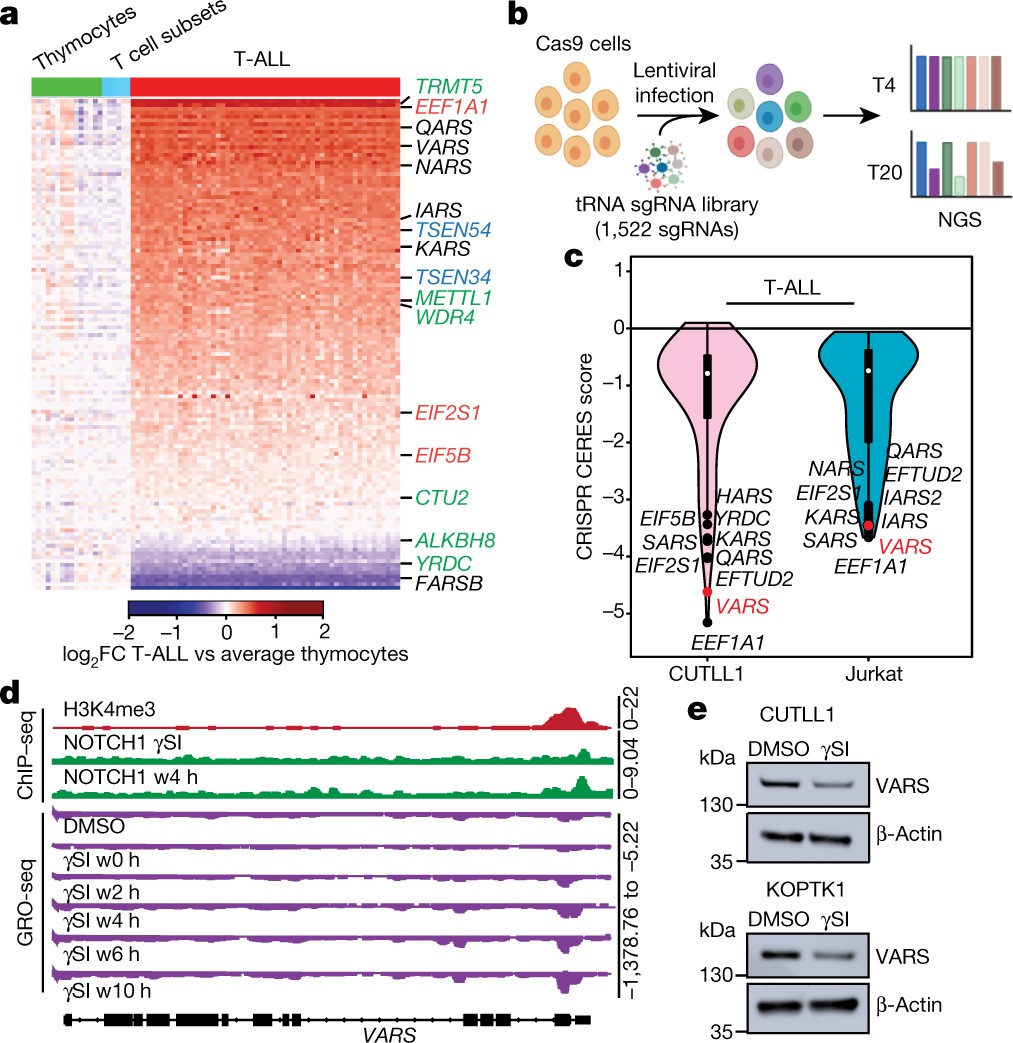
1)研究人员使用CRISPR-Cas9筛选,关注了与转运RNA(tRNA)生物生成有关的基因,并确定了缬氨酸tRNA生物生成的改变增强T细胞急性淋巴细胞白血病(T-ALL)中线粒体生物能的机制。
2)缬氨酸氨酰tRNA合成酶的表达被NOTCH1转录上调,NOTCH1是T-ALL的一个关键肿瘤基因,这强调了肿瘤转录程序在协调tRNA供需方面的作用。
3)通过限制饮食中缬氨酸的摄入量来限制缬氨酸的生物利用度,破坏了小鼠的这种平衡,导致白血病负担减少,体内生存率增加。
4)从机制上讲,缬氨酸限制降低了编码线粒体复合体I亚单位的mRNA翻译率,导致复合体I的组装缺陷和氧化磷酸化受损。
5)在不同的缬氨酸条件下进行的全基因组CRISPR-Cas9功能缺失筛选确定了几个基因,包括SLC7A5和BCL2,其基因消减或药物抑制与缬氨酸限制协同作用,减少T-ALL生长。
本文研究结果表明,tRNA失调是T-ALL发病机制中的一个关键适应因素,并为在血液恶性肿瘤中使用饮食方法来靶向tRNA生物生成提供了分子基础。
参考文献:
Palaniraja Thandapani, et al. Valine tRNA levels and availability regulate complex I assembly in leukaemia. Nature, 2021.
DOI:10.1038/s41586-021-04244-1
https://www.nature.com/articles/s41586-021-04244-1


















