肿瘤源性外体可抑制树突状细胞(DC)和T细胞功能。外源性程序性死亡配体1(PD-L1)的过度分泌导致PD-1/PD-L1免疫治疗的耐药性和临床失败。通过抗外源性PD-L1策略恢复的T细胞可加剧肿瘤细胞的铁下垂,反之亦然。减少外显体抑制并建立抗外显体PD-L1和铁下垂的联系可能挽救令人沮丧的抗肿瘤免疫。有鉴于此,澳门大学的代云路等研究人员,开发了新型光诊疗金属-多酚网络实现抗外泌体PD-L1协同铁死亡增效肿瘤免疫治疗。
本文要点
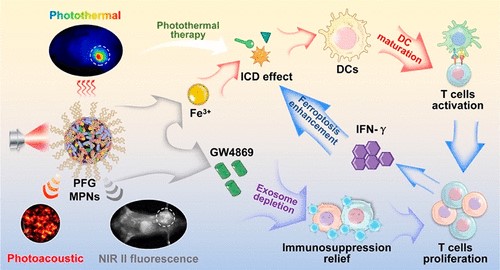
1)研究人员通过封装铁下垂诱导剂(Fe3+)和外显体抑制剂(GW4869)的半导体聚合物组装来构建光疗金属酚网络(PFG MPN)。
2)PFG MPN在精确光热疗法(PTT)中获得了卓越的近红外II荧光/光声成像跟踪性能。
3)PTT增强的免疫原性细胞死亡缓解了DC成熟时的外体沉默。
4)GW4869介导的基于PD-L1的外体抑制使T细胞恢复活力并增强铁下垂。
5)PTT与抗外体PD-L1增强的铁下垂的这种新的协同作用在B16F10肿瘤中诱发有效的抗肿瘤免疫,并对淋巴结转移瘤产生免疫记忆。
参考文献:
Lisi Xie, et al. Phototheranostic Metal-Phenolic Networks with Antiexosomal PD-L1 Enhanced Ferroptosis for Synergistic Immunotherapy. JACS, 2020.
DOI:10.1021/jacs.1c09753
https://pubs.acs.org/doi/10.1021/jacs.1c09753


















